题目内容
8.在标准状况下,224mL某气体的质量为0.40g.试计算这种气体的摩尔质量.分析 根据n=$\frac{V}{{V}_{m}}$计算气体的物质的量,再根据M=$\frac{m}{n}$计算该气体的摩尔质量.
解答 解:标况下,224mL气体的物质的量为$\frac{0.224L}{22.4L/mol}$=0.01mol,其质量为0.40g,故该气体的摩尔质量为$\frac{0.40g}{0.01mol}$=40g/mol,
答:该气体的摩尔质量为40g/mol.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的计算,也可以计算气体的密度,再利用M=ρVm计算.

练习册系列答案
相关题目
18.关于氢键,下列说法正确的是( )
| A. | 每一个水分子内含有两个氢键 | |
| B. | 冰、水和水蒸气中都存在氢键 | |
| C. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
19.配制100mL1.0mol/L 的氢氧化钠溶液,下列操作错误的是( )
| A. | 在托盘天平上放两片大小相同的纸,然后将氢氧化钠放在纸上称取 | |
| B. | 把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,把溶液转入容量瓶 | |
| C. | 用蒸馏水洗涤烧杯、玻棒2~3次,洗涤液也移入容量瓶 | |
| D. | 沿着玻棒往容量瓶中加蒸馏水,接近刻度时,改用胶头滴管滴加直至溶液凹液面的最低点与刻线相切 |
3.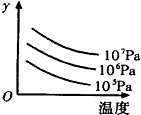 有某可逆反应aA(g)+bB(g)?cC(g);右图表示外界条件(温度、压强)的变化对上述反应的影响.下列判断正确的是( )
有某可逆反应aA(g)+bB(g)?cC(g);右图表示外界条件(温度、压强)的变化对上述反应的影响.下列判断正确的是( )
 有某可逆反应aA(g)+bB(g)?cC(g);右图表示外界条件(温度、压强)的变化对上述反应的影响.下列判断正确的是( )
有某可逆反应aA(g)+bB(g)?cC(g);右图表示外界条件(温度、压强)的变化对上述反应的影响.下列判断正确的是( )| A. | a+b<c时,y轴表示平衡混合气中C的质量分数 | |
| B. | a+b<c时,y轴表示平衡混合气的平均摩尔质量 | |
| C. | △H>0时,y轴表示达到平衡时B的转化率 | |
| D. | △H>0时,y轴表示达到平衡时A的浓度 |
13.下列离子方程式不正确的是( )
| A. | 将氯气溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 向碳酸氢钙溶液中加入过量的氢氧化钠:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+ | |
| D. | 次氯酸钠溶液中通入足量CO2气体:ClO-+CO2+H2O=HClO+HCO3- |
20.下列混合物的分离或提纯的方法不正确的是( )
| A. | 食用花生油中混有水:分液 | |
| B. | 回收碘的CCl4溶液中的CCl4:蒸馏 | |
| C. | 提纯含NaCl杂质的淀粉胶体:过滤 | |
| D. | 从氯化钠溶液中分离出NaCl晶体:蒸发 |
14.结合元素周期律的知识分析下列说法,其中错误的是( )
| A. | Be的氧化物的水化物可能具有两性 | |
| B. | At2为有色固体,HAt不稳定,AgAt感光性很强,既不溶于水也不溶于稀酸 | |
| C. | HClO的酸性一定比H2SO4强 | |
| D. | H2Se是无色、有毒、不如H2S稳定的气体 |