题目内容
13.氢气和氯在点燃条件下反应,在反应过程中,断裂1molH2中的化学键消耗的能量为436kJ,断裂1molCl2中的化学键消耗的能量为243kJ,形成1molHCl中的化学键释放的能量为431kJ.请用此数据估计由Cl2、H2生成1mol HCl时的热效应( )| A. | 放热91.5 kJ | B. | 放热183 kJ | C. | 吸热183 kJ | D. | 吸热91.5 kJ |
分析 根据反应热等于反应物的总键能-生成物的总键来解答.
解答 解:H2(g)+Cl2(g)=2HCl(g)的反应热=反应物的总键能-生成物的总键能=436kJ•mol-1+243kJ•mol-1-2×431 kJ•mol-1=-183kJ•mol-1,故1mol氢气与1mol氯气反应时放出热量为183kJ,
故选B.
点评 本题主要考查了反应热的计算,难度不大,根据课本知识即可完成.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
8. Ⅰ.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
Ⅰ.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应是放热反应(填放热或吸热).
(2)实验结果表明,催化剂的催化效果与接触面积 有关.
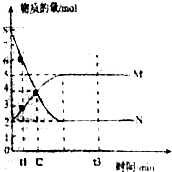
Ⅱ.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中$\frac{a}{b}$=$\frac{2}{1}$
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:$\frac{1}{({t}_{2}-{t}_{1})V}$mol•L-1•min-1
(3)平衡时,N的转化率为75%.
(4)下列叙述中能说明上述反应达到平衡状态的是CE
A.反应中M与N的物质的量之比为1:1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗amolN,同时生成bmolM
E.混合气体的压强不随时间的变化而变化.
 Ⅰ.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
Ⅰ.某实验小组对H2O2的分解做了如下探究.下表是该实验小组研究H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15mL 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(2)实验结果表明,催化剂的催化效果与接触面积 有关.
Ⅱ.一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中$\frac{a}{b}$=$\frac{2}{1}$
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:$\frac{1}{({t}_{2}-{t}_{1})V}$mol•L-1•min-1
(3)平衡时,N的转化率为75%.
(4)下列叙述中能说明上述反应达到平衡状态的是CE
A.反应中M与N的物质的量之比为1:1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗amolN,同时生成bmolM
E.混合气体的压强不随时间的变化而变化.
5.若发现114号元素X,它的最外层有4个电子,则下列有关它的叙述正确的是( )
| A. | X的气态氢化物的稳定性比甲烷强 | B. | X的最高价氧化物是XO2 | ||
| C. | X应为非金属元素 | D. | X的最高价氧化物的水化物是强酸 |
2.下列说法正确的是( )
| A. | 若完全燃烧,1 mol雄酮( )比雌酮( )比雌酮( )多消耗2 mol O2 )多消耗2 mol O2 | |
| B. | 苯分子中的一个碳原子被一个氮原子代替,则新分子的式量为79 | |
| C. | 蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,均能发生银镜反应 | |
| D. | 只用溴水一种试剂不能鉴别甲苯、己烯、乙醇、四氯化碳四种液体 |
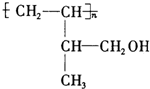
3.下列反应生成的有机物为纯净物的是( )
| A. | 甲烷和氯气光照 | B. | 氯乙烯的加聚 | ||
| C. | 溴乙烷和氢氧化钠水溶液加热 | D. | 丙烯和氯化氢加成 |

 CH3COOCH2CH2CH3+H2O.
CH3COOCH2CH2CH3+H2O. 或
或 .
. .
.
 .
. .
. ;
;