��Ŀ����
����Ŀ����֪A��B��R��D�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵ�ԭ��ϵ��������������AԪ�ػ�̬ԭ�ӵ�һ�����ܱ�BԪ�ػ�̬ԭ�ӵĵ�һ�����ܴ�B�Ļ�̬ԭ�ӵ�L�㡢R��̬ԭ�ӵ�M�����2�������ӣ�D�ǵڢ�����ԭ��������С��Ԫ�ء�
(1)д����̬Dԭ�ӵĵ����Ų�ʽ__________��
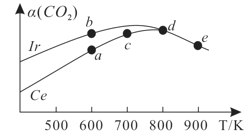
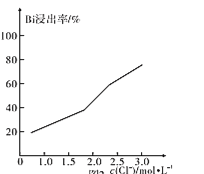
(2)��֪�ߴ���R�ĵ������ִ���Ϣ����������Դ�����о��м�Ϊ��Ҫ�ĵ�λ����ҵ�������ߴ���R�ĵ��ʹ������£�
![]()
д�����̢۵ķ�Ӧ����ʽ___________����֪RHCl3�ķе���31.5oC��������ʵľ���������__________������ԭ�ӵĹ���ӻ�����Ϊ__________�������ʵĿռ乹����______��
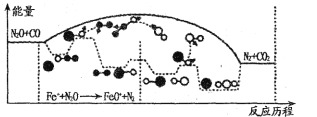
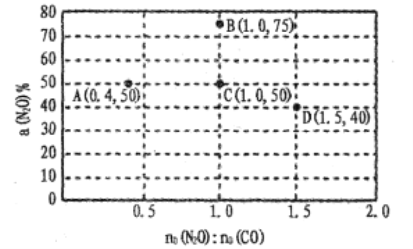
(3)A�ĵ�һ�����ܱ�B�ĵ�һ�����ܴ��ԭ����_________��A��B��Ԫ�طֱ���R�γɵĹ��ۼ��У����Խ�ǿ����________��A��B��Ԫ�ؼ����γɶ��ֶ�Ԫ�����������A3-��Ϊ�ȵ���������ʵĻ�ѧʽΪ_______��
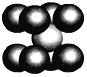
(4)��֪D���ʵľ�����ͼ��ʾ��������Dԭ�ӵ���λ��Ϊ______��һ��D�ľ�������Ϊ____����֪Dԭ�Ӱ뾶Ϊr pm����þ����Ŀռ�������Ϊ_____________ (д���������)��
���𰸡�[Ar]3d64s2 SiHCl3 + H2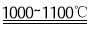 Si + 3HCl ���Ӿ��� sp3 �������� Nԭ�ӵ�2p�ܼ����ڽ��ȶ��İ����״̬ Si-O�� N2O 8
Si + 3HCl ���Ӿ��� sp3 �������� Nԭ�ӵ�2p�ܼ����ڽ��ȶ��İ����״̬ Si-O�� N2O 8 ![]() ��������ԭ��ռ�ݵ����Ϊ������ԭ�ӵ��������ԭ�ӵİ뾶Ϊr pm����ͼ��ʾ���������ⳤΪ=
��������ԭ��ռ�ݵ����Ϊ������ԭ�ӵ��������ԭ�ӵİ뾶Ϊr pm����ͼ��ʾ���������ⳤΪ=![]() �����������=(
�����������=(![]() )3���ռ�������=
)3���ռ�������=![]() =
=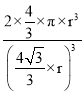 ��100%=68%
��100%=68%
��������
B�Ļ�̬ԭ�ӵ�L�㡢R��̬ԭ�ӵ�M�����2�������ӣ�����������������Ϊ4��6��B����ΪC��OԪ�أ�R����ΪSi��SԪ�أ�D�ǵڢ�����ԭ��������С��Ԫ�أ�ӦΪFe��AԪ�ػ�̬ԭ�ӵ�һ�����ܱ�BԪ�ػ�̬ԭ�ӵĵ�һ�����ܴ���A��ԭ������С��B����A��NԪ�ء�B��OԪ�أ��ߴ���R�ĵ������ִ���Ϣ����������Դ�����о��м�Ϊ��Ҫ�ĵ�λ����R��SiԪ�أ�
(1)D��FeԪ�أ���ԭ�Ӻ�����26�����ӣ����ݹ���ԭ����д��̬Dԭ�ӵĵ����Ų�ʽ��
(2)SiO2��C�ڸ����·����û���Ӧ���ɴ�Si���ֹ��HCl��300�������·�Ӧ����SiHCl3��SiHCl3����������1000��-1100�������·�Ӧ���ɴ��裬�۵ķ�ӦΪSiHCl3�������ķ�Ӧ������Si��HCl�����Ӿ����۷е�ϵͣ��÷�����Siԭ�Ӽ۲���ӶԸ�����4�Ҳ��µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Siԭ�ӵĹ���ӻ����ͼ��ռ乹�ͣ�
(3)ԭ�ӹ���е��Ӵ���ȫ����ȫ�ջ�������ȶ���N��O��Ԫ�طֱ���Si�γɵĹ��ۼ��У�Ԫ�صķǽ�����Խǿ�����γɵĻ������м��Լ��ļ���Խǿ���ȵ�������ԭ�Ӹ�����ȼ��۵�������ȣ�
(4)�þ��������������������þ�����Feԭ�Ӹ���=1+8��![]() =2�����������8��ÿ��Feԭ�ӵ�����=
=2�����������8��ÿ��Feԭ�ӵ�����=![]() ����þ���������������Feԭ���������ռ������� =
����þ���������������Feԭ���������ռ������� =![]() ��
��
(1)D��FeԪ�أ���ԭ�Ӻ�����26�����ӣ����ݹ���ԭ����д��̬Dԭ�ӵĵ����Ų�ʽΪ[Ar]3d64s2��
(2)SiO2��C�ڸ����·����û���Ӧ���ɴ�Si���ֹ��HCl��300�������·�Ӧ����SiHCl3��SiHCl3����������1000��-1100�������·�Ӧ���ɴ��裬�۵ķ�ӦΪSiHCl3�������ķ�Ӧ������Si��HCl����Ӧ����ʽΪSiHCl3 +H2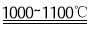 Si+3HCl�����Ӿ����۷е�ϵͣ��������۷е�ϵͣ�������ʾ�������Ϊ���Ӿ��壬�÷�����Siԭ�Ӽ۲���ӶԸ�����4�Ҳ����µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Siԭ�ӵĹ���ӻ����ͼ��ռ乹�ͷֱ�Ϊsp3���������Σ�
Si+3HCl�����Ӿ����۷е�ϵͣ��������۷е�ϵͣ�������ʾ�������Ϊ���Ӿ��壬�÷�����Siԭ�Ӽ۲���ӶԸ�����4�Ҳ����µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Siԭ�ӵĹ���ӻ����ͼ��ռ乹�ͷֱ�Ϊsp3���������Σ�
(3)ԭ�ӹ���е��Ӵ���ȫ����ȫ�ջ�������ȶ���Nԭ�ӵ�2p�ܼ����ڽ��ȶ��İ����״̬������Nԭ�ӱ�Oԭ�ӵ�һ�����ܴ�N��O��Ԫ�طֱ���Si�γɵĹ��ۼ��У�Ԫ�صķǽ�����Խǿ�����γɵĻ������м��Լ��ļ���Խǿ����ΪOԪ�صķǽ����Դ���N������O-Si����N-Si�����ȵ�������ԭ�Ӹ�����ȼ��۵�������ȣ�N3-�к���3��ԭ�ӡ��۵�������16��������ӻ�Ϊ�ȵ�����ĵ�������ΪN2O��
(4)�þ��������������������þ�����Feԭ�Ӹ���=1+8��![]() =2�������ϵ�Feԭ�ӱ������ϵ�8��ԭ�Ӱ�Χ���������������8��ÿ��Feԭ�ӵ�����=
=2�������ϵ�Feԭ�ӱ������ϵ�8��ԭ�Ӱ�Χ���������������8��ÿ��Feԭ�ӵ�����=![]() g����þ���������������Feԭ������=2��
g����þ���������������Feԭ������=2��![]() g=2��
g=2��![]() g=
g=![]() g����������ԭ��ռ�ݵ����Ϊ������ԭ�ӵ��������ԭ�ӵİ뾶Ϊr pm����ͼ��ʾ���������ⳤΪ=
g����������ԭ��ռ�ݵ����Ϊ������ԭ�ӵ��������ԭ�ӵİ뾶Ϊr pm����ͼ��ʾ���������ⳤΪ=![]() �����������=(
�����������=(![]() )3���ռ�������=
)3���ռ�������=![]() =
=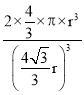 ��100%=68%��
��100%=68%��