题目内容
7.下列化合物分子中的所有原子都处于同一平面的是( )| A. | 间溴甲苯 | B. | 对二甲苯 | C. | 氯乙烯 | D. | 丙烯 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A、间溴甲苯含有1个甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面上,故A错误;
B、对二甲苯含有2个甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面上,故B错误;
C、乙烯具有平面型结构,氯乙烯可看作是一个氯原子取代乙烯中的一个氢原子,在同一个平面,故C正确;
D、丙烯中有一个甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面上,故D错误.
故选C.
点评 本题主要考察有机化合物的结构特点,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列叙述正确的是( )
| A. | 离子化合物中可能含共价键,共价化合物中不含离子键 | |
| B. | 共价化合物中可能含离子键,离子化合物中只含离子键 | |
| C. | 构成单质分子的微粒一定含有共价键 | |
| D. | 双原子分子中的共价键,一定是非极性键 |
11.下列说法中正确的是( )
| A. | 1mol H2约含有6.02×1023个微粒 | |
| B. | 水的摩尔质量是18g | |
| C. | 氯化氢的摩尔质量就是它的相对分子质量 | |
| D. | 相同物质的量的SO2和SO3,含氧原子个数之比为2:3 |
15.已知1mol X2完全燃烧生成X2O(g)放出热量a kJ,且氧气中1mol O═O键完全断裂时吸收能量b kJ,X2O中1mol X-O键形成时放出能量c kJ,X2中1mol X-X键断裂时吸收能量为( )
| A. | (4c-b+2c)kJ | B. | $\frac{4c-b-2a}{2}$ kJ | C. | 4c+b-2a kJ | D. | $\frac{4c+b-2a}{2}$ kJ |
2.依据元素周期表寻找催化剂、耐高温、耐腐蚀的合金材料在( )
| A. | 金属与非金属分界线附近 | B. | 非金属区域 | ||
| C. | 过渡元素 | D. | 左下方的金属元素区域 |
12.若用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1 mol Fe与少量氯气反应时转移的电子数为2NA | |
| B. | 0.2 mol S在空气中充分燃烧,转移电子数为0.6NA | |
| C. | 0.1molCl2溶于水中发生反应,转移电子数为0.1NA | |
| D. | 1.5 mol Na2O2与足量的二氧化碳充分反应,转移电子数为1.5NA |
16.下列说法正确的是( )
| A. | 控制塑料购物袋的使用主要是为了节约成本 | |
| B. | 使用可降解塑料袋有利于减少“白色污染” | |
| C. | 聚氯乙烯塑料袋可用来长时间存放食品 | |
| D. | 塑料购物袋具有热固性,不能回收利用 |
 (1)熔点沸点HF>HI;原因:HF分子间含有氢键
(1)熔点沸点HF>HI;原因:HF分子间含有氢键 .
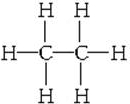
.
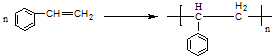 .
.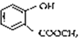 含有的官能团的名称为酚羟基、酯基.
含有的官能团的名称为酚羟基、酯基.