题目内容
7.硫酸铜是一种用途广泛的化工原料.某学习小组把适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全.通过蒸发、结晶得到硫酸铜晶体(装置如图I、Ⅱ所示)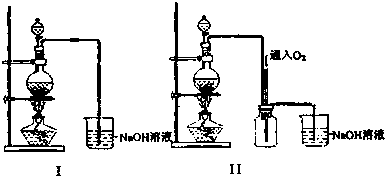
(1)烧瓶中发生反应的化学方程式为3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O.
(2)图Ⅱ是图I的改进装置.其优点有增加了安全瓶;有利于有毒气体被完全吸收.
(3)为符合绿色化学的要求,该学习小组进行了如下探究:将氧气直接通入到铜粉与稀硫酸的混合物中,发现常温下几乎不反应,但向混合物中加入FeSO4后再通入氧气,反应则立即发生.
①试用离子方程式表示反应发生的原理2Cu+4H++O2$\frac{\underline{\;Fe_{2}+\;}}{\;}$2Cu2++2H2O;在该反应中FeSO4的作用是催化剂.
②已知pH≥4.4时Cu2+以Cu(OH)2的形式开始沉淀,pH≥6.4时完全沉淀;Fe(OH)3完全沉淀时的pH为3.7,又测得反应完成后溶液呈强酸性.请设计一个除去所得溶液中杂质离子的实验方案向反应后的溶液中加入CuO[或Cu(OH)2或CuCO3],调节溶液的pH3.7~4.4,将沉淀滤去.
(4)为寻找更加适宜的氧化剂,该小组又进行了如下探究:称量3.2g铜丝放到45mL 1.5mol•L-1的稀硫酸中,控温在50℃,加入18mL 10%的H2O2,反应30min后升温到60℃,持续反应1小时后铜丝反应完全.蒸发、冷却、结晶,过滤时用少量95%的酒精淋洗晾干,得到10g CuSO4•5H2O.
①该实验铜丝被氧化的原理是(用离子方程式袭示)Cu+H2O2+2H+═Cu2++2H2O.
②反应过程中温度不宜过高的原因是防止双氧水分解,过滤时采用酒精淋洗的优点是酒精极易蒸发带走水分,加速晶体晾干,减少晶体的溶解;该小组得到硫酸铜晶体的实际产率是80%.
分析 (1)烧瓶中发生Cu与稀硝酸的氧化还原反应;
(2)图Ⅱ中中间的装置可防止倒吸,并发生氮的氧化物与水的反应;
(3)①在酸性条件下,铜单质能被氧气氧化为铜离子;
②调节溶液的pH3.7~4.4;
(4)①铜在酸性条件能被双氧水氧化;
②过氧化氢不稳定,温度过高易分解生成水和氧气;酒精极易蒸发带走水分;根据铜原子守恒得铜和五水硫酸铜的关系,求出CuSO4•5H2O 质量,然后求出产率.
解答 解:(1)烧瓶中发生Cu与稀硝酸的氧化还原反应,化学方程式为3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
或Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O;
(2)由装置比较可知,图Ⅱ中多出的装置能①溶液不导管不直接接触,防止倒吸,②NO与氧气及碱反应,使有害气体能被完全吸收,故答案为:增加了安全瓶;有利于有毒气体被完全吸收;
(3)①在酸性条件下,铜单质能被氧气氧化为铜离子,离子方程式:2Cu+4H++O2$\frac{\underline{\;Fe_{2}+\;}}{\;}$2Cu2++2H2O,FeSO4作催化剂,故答案为:2Cu+4H++O2$\frac{\underline{\;Fe_{2}+\;}}{\;}$2Cu2++2H2O或4Fe2++O2+4H+═4Fe3++2H2O,2Fe3++Cu═2Fe2++Cu2+;催化剂;
②加入CuO[或Cu(OH)2或CuCO3],调节溶液的pH3.7~4.4,将沉淀滤去,故答案为:向反应后的溶液中加入CuO[或Cu(OH)2或CuCO3],调节溶液的pH3.7~4.4,将沉淀滤去;
(4)①铜在酸性条件能被双氧水氧化,离子方程式Cu+H2O2+2H+═Cu2++2H2O,故答案为:Cu+H2O2+2H+═Cu2++2H2O;
②根据双氧水加热易分解的性质分析,过氧化氢不稳定,温度过高易分解生成水和氧气;酒精极易蒸发带走水分,加速晶体晾干,减少晶体的溶解;设3.2g铜生成五水硫酸铜的质量为xg,根据铜原子守恒得铜和五水硫酸铜的关系式为:
Cu→CuSO4•5H2O
64g 250g
3.2g xg
所以x=12.5
理论上生成CuSO4•5H2O 12.5克,故产率为$\frac{10g}{12.5g}$×100%=80%,故答案为:防止双氧水分解;酒精极易蒸发带走水分,加速晶体晾干,减少晶体的溶解;80%.
点评 本题考查硫酸铜制备实验方案的设计,明确装置的作用及发生的氧化还原反应是解答本题的关键,注意除杂的方法及物质的成分、性质的差异、盐类水解的知识来解答,综合性较强,题目难度较大.

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案| A. | 8.5g | B. | 10.8g | C. | 6.2g | D. | 4.6g |
将0.1mol•L﹣1的KI溶液和0.05mol•L﹣1 Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I﹣ 2Fe2++I2”的是( )
2Fe2++I2”的是( )
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成(用于证明Fe2+存在) |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A.①和② B.②和④ C.②和③ D.①和③
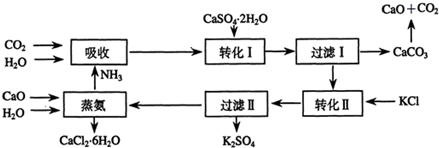
(1)在这个工艺中,有很多粒子都具有相同的电子数.
写出该工艺中具有相同电子数的四种粒子的化学式:NH3、H2O、NH4+、OH-、H3O+五种的任意四种.
(2)1919年由Langmuir提出了等电子体.原子数相同、电子数相同的粒子,互称为等电子体.A、B、C、D、E、F 是原子序数依次增大的6种位于元素周期表前20号的元素.B、C、D、E位于同周期.C是构成空气的主要元素.F与B、D都可形成XY2型离子化合物FB2、FD2,且都可与A2D(无色液体)反应放出气体.B22-与C2是等电子体,D22-与E2是等电子体.F原子的N层电子数与K层电子数相同.
①比较C、D、E对应的简单阴离子的半径(用离子符号表示)N3->O2->F-(由大到小);
②写出能证明D和E非金属性强弱的一个化学方程式2F2+2H2O=4HF+O2.
③由上述6种元素中的4种构成的离子化合物是(写出两种)NH4HCO3、(NH4)2CO3、Ca(HCO3)2、(CH3COO)2Ca其中两种,其中所含的化学键类型有离子键、共价键.
(3)①过滤Ⅱ所得滤液中大量含有的阳离子有哪些?请分别检验.(可不填满下表)
| 所含离子 | 检验方法 |
| K+ | 取少量滤液于试管中,通过焰色反应,火焰呈紫色(透过蓝色钴玻璃) |
| NH4+ | 取少量滤液于试管中,并向其中加入NaOH微热,有刺激性气味产生(该气体可使湿润红色石蕊试纸变蓝) |
| A. | 需要持续加热才能发生的反应一定是吸热反应 | |
| B. | MnO2能加速H2O2的分解,是因为MnO2可以降低反应所需的活化能 | |
| C. | 分别稀释10mLpH=1的盐酸和醋酸至100mL,后者pH变化大,说明醋酸是弱酸 | |
| D. | 向橙色的K2Cr2O7溶液中滴加NaOH溶液,溶液颜色变黄,说明化学平衡发生了移动 |
| A. | 同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl④NH3•H2O,c(NH4+)由大到小的顺序是:①>③>②>④ | |
| B. | 常温时,将等体积的盐酸和氨水混合后,pH=7,则c (NH4+)>c (Cl-) | |
| C. | 0.2 mol•L-1Na2CO3溶液中:c (OH-)=c (HCO3-)+c (H+)+c (H2CO3) | |
| D. | 0.01 mol•L-1的NH4Cl溶液与0.05mol•L-1的NaOH溶液等体积混合:c (Cl-)>c (NH4+)>c (Na+)>c (OH-)>c (H+) |
| A. | 质量是4g | B. | 标准状况下的体积约为33.6L | ||
| C. | 电子数是3mol | D. | 分子数是9.03×1023 个 |
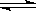 3C(g)+2D(s) △H>0。达到平衡时生成
3C(g)+2D(s) △H>0。达到平衡时生成 了1.8 mol C。
了1.8 mol C。