题目内容
在一定温度下,向一固定容积的密闭容器中加入 1mol A和 2mol B,发生下述反应:A(g)+2B(g) 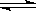 3C(g)+2D(s) △H>0。达到平衡时生成
3C(g)+2D(s) △H>0。达到平衡时生成 了1.8 mol C。
了1.8 mol C。
(1)在相同条件下,若向该容器中改为加入0.3mol A、0.6 mol B,要使平衡混合气体中C物质的体积分数与原平衡的相同,在D足量时,则还应加入 mol的物质C。
(2)若维持容器的体积和温度不变,反应从逆反应方向开始,按不同的配比作为起始物质,达到平衡时C仍为1.8 mol 。则D的起始物质的量n(D)应满足的条件是:n(D)___________。
当改变温度或压强时,有可能改变物质的聚集状态,对平衡产生影响。回答(3)(4)
(3)若升高平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的平均相对分子质量未发生改变,试解释形成这种结果的可能原因是:_________________;
(4)若将容器改为容积可变的容器,在一定温度和常压下,建立上述平衡之后,A的物质的量浓度为a mol/L。现持续增大压强,当:
①当压强为原来1.5倍时,A的平衡时物质的量浓度为m mol/L,测得m=1.5a;
②当压强为原来10倍时,A的平衡时物质的量浓度为n mol/L,测得n >10 a;
③当压强为原来100倍时,A的平衡时物质的量浓度为p mol/L,测得p<100a。
试解释形成这种结果的可能的原因:
①1.5倍时: ;
②10倍时: ;
③100倍时:  。
。
练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
8.影响化学反应速率的因素很多,下列措施一定能加快化学反应速率的是( )
| A. | 升高温度 | B. | 增大压强 | C. | 降低温度 | D. | 改变反应物用量 |
9.下列叙述不正确的是( )
| A. | 符合通式:CnH2n-2的有机物一定是炔烃 | |
| B. | 乙炔分子中碳碳叁键的键能不是碳碳单键和碳碳双键的键能之和 | |
| C. | 等质量的烃中含氢量越高,充分燃烧时,消耗的氧气越多 | |
| D. | 1-丁炔分子中的四个碳原子在同一条直线上 |


 的电离受到抑制
的电离受到抑制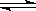 Na2S(s)+4H2O(g).下列说法正确的是( )
Na2S(s)+4H2O(g).下列说法正确的是( )