题目内容
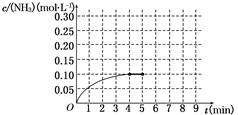
在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g) 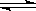 2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示。反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示。反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
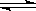 2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示。反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示。反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
| A.0.20 mol·L-1 | B.0.12 mol·L-1 |
| C.0.10 mol·L-1 | D.0.08 mol·L-1 |
A
试题分析:N2(g)+3H2(g)
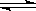 2NH3(g) ,假设0.2 mol的N2和0.6 mol的H2全部反应,则生产的氨气的物质的量为0.4mol,即氨气的物质的量浓度为0.4/2="0.20" mol·L-1,由于该反应为可逆反应,所以反应达到平衡后,第5分钟末,保持其它条件不变,只改变反应温度,不可能使反应达到100%,故NH3的物质的量浓度不可能为0.20 mol·L-1,所以答案选A。
2NH3(g) ,假设0.2 mol的N2和0.6 mol的H2全部反应,则生产的氨气的物质的量为0.4mol,即氨气的物质的量浓度为0.4/2="0.20" mol·L-1,由于该反应为可逆反应,所以反应达到平衡后,第5分钟末,保持其它条件不变,只改变反应温度,不可能使反应达到100%,故NH3的物质的量浓度不可能为0.20 mol·L-1,所以答案选A。点评:本题考查了可逆反应,该考点是高考考查的重点,本题要理解可逆反应不可能100%进行,本题比较容易。

练习册系列答案
相关题目
 pC(g)+qD(g),C物质的质量分数[w(C)]与温度、压强的关系如图所示,下列判断正确的是( )
pC(g)+qD(g),C物质的质量分数[w(C)]与温度、压强的关系如图所示,下列判断正确的是( )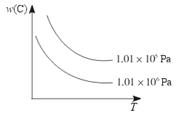
 2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。 C(g)+D,A和C均为无色气体,当反应达到平衡时,下列叙述不正确的是( )
C(g)+D,A和C均为无色气体,当反应达到平衡时,下列叙述不正确的是( ) 2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL,生成0.4moLC, 则下列计算结果不正确的是( )
2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL,生成0.4moLC, 则下列计算结果不正确的是( ) eC(g)+fD(g)在反应过程中,当其他条件不变时,C的体积分数
eC(g)+fD(g)在反应过程中,当其他条件不变时,C的体积分数 (C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是 ( )
(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示。下列叙述正确的是 ( )
 C (g) + D(g),能说明该反应达到化学平衡状态的是
C (g) + D(g),能说明该反应达到化学平衡状态的是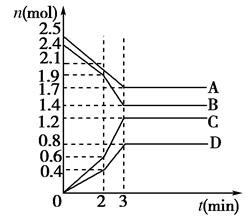
 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率 、 。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·L-1。计算该条件下反应的平衡常数K和SO2的平衡转化率 、 。