题目内容
2.下列各项中,不能说明2HI?H2+I2(g)已经达到平衡状态的是( )| A. | 单位时间内,生成nmolH2的同时生成nmolHI | |
| B. | 一个H-H键断裂的同时,有2个H-I键断裂 | |
| C. | 温度和体积一定时,某一生成物浓度不再变化 | |
| D. | 温度和体积一定时,混合气体的颜色不再变化 |
分析 反应到达平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各物质的浓度、百分含量不变,可以及由此衍生的一些量也不发生变化,由此进行判断.解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、单位时间内,生成nmolH2的同时生成2nmolHI,才能说明正逆反应速率相等,故A选;
B、一个H-H键断裂的同时,有2个H-I键断裂,不能说明正逆反应速率相等,故B不选;
C、温度和体积一定时,某一生成物浓度不再变化,是化学平衡的特征,故C不选;
D、混合气体的颜色不再变化,说明I2的浓度不再变化,反应到达平衡,故D不选.
故选A.
点评 本题主要考查平衡平衡状态的判断,可以抓住本质特征:υ正=υ逆(同种物质),解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.

练习册系列答案
相关题目
13.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1 mol•L-1 HA溶液与0.1 mol•L-1 NaOH溶液混合至溶液呈中性:c(Na+)>c(A-) | |
| B. | 0.1 mol•L-1 HA溶液中:c(H+)=c(OH-)+c(A-) | |
| C. | 0.1 mol•L-1 NaA溶液中:c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液中加入少量NaA固体,HA的电离常数减小 |
17.据报道,某些花岗岩会产生放射性元素氡(${\;}_{86}^{222}$Rn),下列说法中不正确的是( )
| A. | 该原子的质量数为222 | B. | Rn是86号元素 | ||
| C. | 一个222 86Rn原子中有136个中子 | D. | 一个222 86Rn原子中有136个电子 |
14.化学实验有助于理解化学知识,形成化学观念.下列实验操作正确的是( )
| A. |  称量药品 | B. | 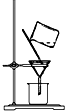 过滤 | C. | 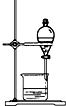 分离乙醇和水 | D. | 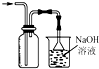 收集氯气 |
11.已知,H2和I2反应的历程为:①I2+M?2I•+M慢 ②H2+2I•→2HI快式中M是指反应器壁或其他惰性分子,不参与反应,只具有传递能量的作用.下列关于该反应的说法正确的是( )
| A. | 反应速率与I•的浓度有关 | B. | M是该反应的催化剂 | ||
| C. | 反应①与②的活化能相等 | D. | v(H2)=v(I2)=v(HI) |