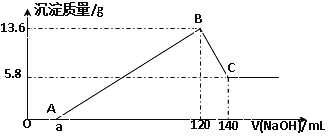
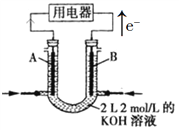
【题目】钢铁分析中常用高氯酸(HClO4)溶解矿样,某研究性学习小组欲制取少量高氯酸。该学习小组查阅到:
a.HClO4浓度高于60%时遇含碳化合物易爆炸,浓度低于60%时比较稳定;
b.NaClO4与浓硫酸反应可制得高氯酸,若采用真空蒸馏可得纯高氯酸;
c.NaClO3在673K(400℃) 分解产生NaClO4、NaCl和一种气体。
该小组同学设计实验分三步制备高氯酸:
(一)制氯气并使制得的氯气与氢氧化纳溶液反应制氯酸纳;
(二)氯酸钠分解制高氯酸钠;
(三)高氯酸纳与浓硫酸反应制高氯酸[2NaClO4+H2SO4(浓) Na2SO4+2HClO4]。
Na2SO4+2HClO4]。
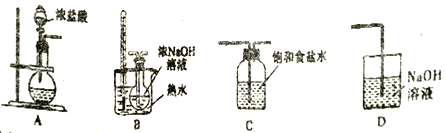
(1)制取氯酸钠的装置连接顺序为A,___________
(2)B 装置中发生反应的离子方程式为__________________________。
(3)为了制备高氯酸钠并推出氯酸钠分解制高氯酸钠的化学方程式,该小组设计了两组装置(甲,乙)如下:
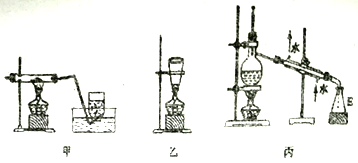
该小组经过分析决定选用甲装置制备高氯酸钠,取NaClO3样品2.13 g,加热充分反应后集气瓶中收集到224 mL (标准状况下)气体,则该反应的化学方程式为_________________________;不选用乙装置的原因可能为______________________。
(4)用丙裝置制备高氯酸,向烧瓶中加入高氯酸钠,然后加入浓硫酸后,加热可制取高氯酸。实验开始前,胶塞及导管接口需要包锡箔纸,其原因是___________,仪器E的名称为___________。该组同学发现操作中少加入一种物质,该物质的名称为___________。发现后的正确操作为_________________。
(5)工业上大量制备NaClO4常用高电流密度电解NaClO3的方法,试写出以惰性电极电解时的阳极反应式:_______________________________________________。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案