题目内容
【题目】C、N、S 的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)CO2 的重整用 CO2 和 H2 为原料可得到 CH4 燃料。
已知: ①CH4 (g)+CO2(g)=2CO(g)+2H2(g) △H1=+247kJ/mol
②CH4 (g)+H2O(g)=CO(g)+3H2(g) △H2=+205kJ/mol
写出 CO2 重整的热化学方程式:_____。
(2) “亚碳酸盐法”吸收烟中的 SO2
①将烟气通入 1.0mol/L 的 Na2SO3 溶液,若此过程中溶液体积不变,则溶液的 pH 不断_____(填“减小”“不变” 或“增大)。当溶液 pH 约为 6 时,吸收 SO2 的能力显著下降,应更换吸收剂,此时溶液中 c(SO32-) =0.2mol/L, 则溶液中 c(HSO3-) =_____。
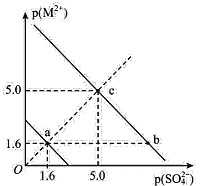
②室温条件下,将烟气通入(NH4)2SO3 溶液中,测得溶液 pH 与各组分物质的量分数的变化关系如图: b 点时溶液 pH=7,则 n(NH4+):n(HSO3—)= ______________ 。

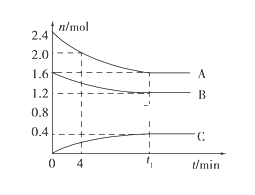
(3)催化氧化法去除 NO。一定条件下,用 NH3 消除 NO 污染,其反应原理4NH3+6NO![]() 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:

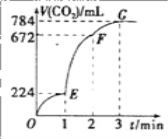
①曲线 a 中,NO 的起始浓度为6×10-4mg·m-3,从 A 点到 B 点经过0.8s,该时间段内 NO 的脱除速率为_____mg·m-3·s-1。
②曲线 b 对应 NH3 与 NO 的物质的量之比是_____。
(4)间接电化学法除 NO。其原理如图所示:写出阴极的电极反应式(阴极室溶液呈酸性)_____。吸收池中除去 NO 的原理_____(用离子方程式表示)。

【答案】CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=163kJ/mo1 减小 1.6mol/L 3:1 1.5×104 3:1 ![]()
![]()
【解析】
(1)已知:①CH4 (g)+CO2(g)=2CO(g)+2H2(g) △H1=+247k/mol,
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+205k/mol,
根据盖斯定律,①-②×2得:CO2(g)+4H2(g)=CH4(g)+2H2O(g),据此计算△H;
(2)①二氧化硫通入亚硫酸钠溶液生成亚硫酸氢钠,亚硫酸氢钠显酸性,据此分析;根据反应方程式的量的关系计算可得;
②先判断溶质,写出电荷守恒式,在利用pH=7时,c(H+)=c(OH-)找出其他离子的等量关系,结合图示进行等量删减或替换,最后得出结果;
(3)①曲线a中,NO的起始浓度为6×10-4mgm-3,根据图象得到A、B处的NO脱除率,可得两处的NO的浓度,再计算脱除速率;
②NH3与NO的物质的量的比值越大,NO的脱除率越大,据此分析;
(4)阴极得到电子发生还原反应,结合酸性环境书写;阴极产物吸收NO。
(1)已知:①CH4(g)+CO2(g)=2CO(g)+2H2(g) △H1=+247k/mol,
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+205k/mol,
根据盖斯定律,由①②×2得反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=△H12△H2=163kJ/mo1,
故答案为:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H=163kJ/mo1;
(2)①将烟气通入1.0mol/L的Na2SO3溶液,二氧化硫与亚硫酸钠和水反应生成亚硫酸氢钠,亚硫酸氢钠以电离为主,显酸性,故溶液pH不断减小;向亚硫酸钠溶液中通入二氧化硫生成亚硫酸氢钠,反应方程式SO2+Na2SO3+2H2O=2NaHSO3,溶液中反应的亚硫酸根离子和生成亚硫酸氢根离子的物质的量比为1:2,即溶液中参加反应的亚硫酸根为(1.00.2)mol/L,则生成c(![]() )=2×(1.00.2)mol/L=1.6mol/L,
)=2×(1.00.2)mol/L=1.6mol/L,
故答案为:减小;1.6mol/L;
②b点时溶液pH=7,此时溶液中的溶质是(NH4)2SO3和NH4HSO3,根据电荷守恒:c(![]() )+c(H+)=c(OH)+c(
)+c(H+)=c(OH)+c(![]() )+2c(
)+2c(![]() ),因pH=7,故c(H+)=c(OH),则c(
),因pH=7,故c(H+)=c(OH),则c(![]() )=c(
)=c(![]() )+2c(
)+2c(![]() ),由图可读出b点时,c(
),由图可读出b点时,c(![]() )=c(
)=c(![]() ),则c(
),则c(![]() )=3 c(
)=3 c(![]() ),因在同一体系,n(
),因在同一体系,n(![]() ):n(
):n(![]() )=3:1,
)=3:1,
故答案为:3:1;
(3)①曲线a中,NO的起始浓度为6×104mgm3,A点的脱除率为55%,B点的脱除率为75%,从A点到B点经过0.8s,该时间段内NO的脱除速率为6×104mgm3×(0.750.55)÷0.8s=1.5×104mgm3s1,
故答案为:1.5×104;
②NH3与NO的物质的量的比值越大,NO的脱除率越大,则物质的量之比分别为4:1,3:1,1:3时,对应的曲线为a,b,c,即曲线b对应的物质的量之比是3:1,
故答案为:3:1;
(4)阴极得到电子发生还原反应,根据图可知是![]() 在酸性条件下发生还原反应,生成
在酸性条件下发生还原反应,生成![]() ,其电极反应式为
,其电极反应式为![]() ;根据图示,吸收池中
;根据图示,吸收池中![]() 和NO是反应物,N2和
和NO是反应物,N2和![]() 是生成物,则吸收池中除去NO的原理是:
是生成物,则吸收池中除去NO的原理是:![]() ,
,
故答案为:![]() ;
;![]() 。
。

【题目】含有K2Cr2O7的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有 K2Cr2O7 的废水并回收重铬酸,具体的流程如下:
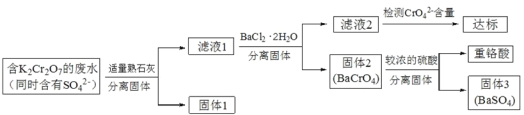
已知:CaCr2O7、BaCr2 O7 易溶于水,其它几种盐在常温下的溶度积如下表所示。
物质 | CaSO4 | CaCrO4 | BaCrO4 | BaSO4 |
溶度积 | 9.1106 | 2.30 102 | 1.17 1010 | 1.08 1010 |
(1)用离子方程式表示K2Cr2O7溶液中同时存在 K2CrO4的原因(将离子方程式补充完整):______Cr2O72-+______![]() ____CrO42+______
____CrO42+______
(2)向滤液 1 中加入 BaCl2 ![]() 2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
①结合上述流程说明熟石灰的作用:_____。
②结合表中数据,说明选用Ba2 不选用Ca2处理废水的理由:_____。
③ 研究温度对CrO42 沉淀效率的影响。实验结果如下:在相同的时间间隔内,不同温度下CrO42- 的沉淀率(沉淀率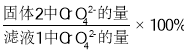 如图所示)
如图所示)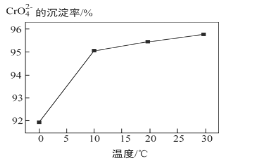
已知:![]()
CrO42- 的沉淀效率随温度变化的原因是_____。
(3)向固体2中加入硫酸,回收重铬酸。
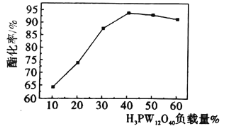
①硫酸浓度对重铬酸的回收率如下图(左)所示。结合化学平衡移动原理,解释使用 0.450 mol/L 的硫酸时,重铬酸的回收率明显高于使用 0.225 mol/L 的硫酸的原因:_____。
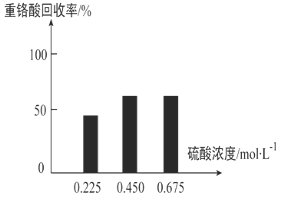
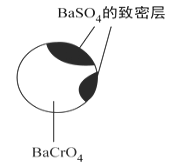
②回收重铬酸的原理如上图(右)所示。当硫酸浓度高于0.450 mol/L时,重铬酸的回收率没有明显变化,其原因是_____。
(4)综上所述,沉淀BaCrO4进一步回收重铬酸的效果与_____、_____、有关。