题目内容
【题目】含有K2Cr2O7的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有 K2Cr2O7 的废水并回收重铬酸,具体的流程如下:
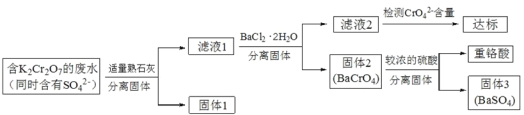
已知:CaCr2O7、BaCr2 O7 易溶于水,其它几种盐在常温下的溶度积如下表所示。
物质 | CaSO4 | CaCrO4 | BaCrO4 | BaSO4 |
溶度积 | 9.1106 | 2.30 102 | 1.17 1010 | 1.08 1010 |
(1)用离子方程式表示K2Cr2O7溶液中同时存在 K2CrO4的原因(将离子方程式补充完整):______Cr2O72-+______![]() ____CrO42+______
____CrO42+______
(2)向滤液 1 中加入 BaCl2 ![]() 2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
①结合上述流程说明熟石灰的作用:_____。
②结合表中数据,说明选用Ba2 不选用Ca2处理废水的理由:_____。
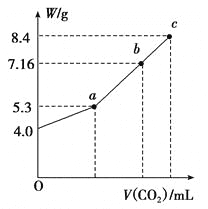
③ 研究温度对CrO42 沉淀效率的影响。实验结果如下:在相同的时间间隔内,不同温度下CrO42- 的沉淀率(沉淀率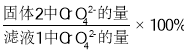 如图所示)
如图所示)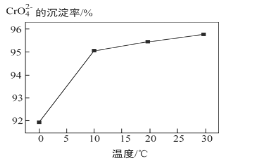
已知:![]()
CrO42- 的沉淀效率随温度变化的原因是_____。
(3)向固体2中加入硫酸,回收重铬酸。
①硫酸浓度对重铬酸的回收率如下图(左)所示。结合化学平衡移动原理,解释使用 0.450 mol/L 的硫酸时,重铬酸的回收率明显高于使用 0.225 mol/L 的硫酸的原因:_____。
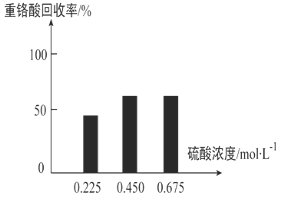
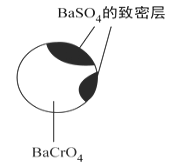
②回收重铬酸的原理如上图(右)所示。当硫酸浓度高于0.450 mol/L时,重铬酸的回收率没有明显变化,其原因是_____。
(4)综上所述,沉淀BaCrO4进一步回收重铬酸的效果与_____、_____、有关。
【答案】1 1H2O 2 2 H+ 沉淀SO42-;调节溶液pH,使Cr2O72-转化为CrO42-而沉淀 温度升高,沉淀速率加快 BaCrO4比CaCrO4更难溶,可以使CrO42-沉淀更完全 c(H2SO4)增大,则c(SO42-)增大,与Ba2+生成沉淀,促进BaCrO4 ![]() Ba2+ +CrO42-平衡右移,c(CrO42-)增大;同时,c(H+)也增大,共同促进Cr2O72-+ H2O
Ba2+ +CrO42-平衡右移,c(CrO42-)增大;同时,c(H+)也增大,共同促进Cr2O72-+ H2O![]() 2CrO42- + 2H+ 平衡左移,有利于生成更多的H2Cr2O7 BaSO4与BaCrO4溶解度接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难于接触H2SO4,阻碍重铬酸生成 溶液pH H2SO4浓度
2CrO42- + 2H+ 平衡左移,有利于生成更多的H2Cr2O7 BaSO4与BaCrO4溶解度接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难于接触H2SO4,阻碍重铬酸生成 溶液pH H2SO4浓度
【解析】
含有K2Cr2O7的废水同时含有SO42,加入适量熟石灰过滤得到的固体1为硫酸钙和滤液1,向滤液1中加入BaCl22H2O的目的是使CrO42从溶液中沉淀出来,过滤得到固体2为BaCrO4,向固体2中加入硫酸,回收重铬酸,同时生成固体3为硫酸钡沉淀。
(1). K2Cr2O7溶液中同时存在K2CrO4的原因是重铬酸根离子在水溶液中存在化学平衡生成铬酸根离子和氢离子,反应的离子方程式为Cr2O72+H2O![]() 2CrO42+2H+;
2CrO42+2H+;
(2). ①.根据表中物质的溶度积常数可知,熟石灰的作用是沉淀硫酸根离子,调节溶液pH使Cr2O72转化为CrO42;
②.根据表中数据可知,BaCrO4比CaCrO4更难溶,所以选用Ba2+处理废水可以使CrO42沉淀更完全;
③.根据图象可知,CrO42的沉淀率随温度升高增大,原因是温度升高,沉淀速率加快;
(3). ①. c(H2SO4)增大,则c(SO42-)增大,与Ba2+生成沉淀,促使BaCrO4(s)![]() Ba2+(aq)+CrO42(aq)平衡右移,使c(CrO42)增大,同时c(H+)也增大,共同促使Cr2O72+H2O
Ba2+(aq)+CrO42(aq)平衡右移,使c(CrO42)增大,同时c(H+)也增大,共同促使Cr2O72+H2O![]() 2CrO42+2H+平衡左移,可以生成更多的H2Cr2O7;
2CrO42+2H+平衡左移,可以生成更多的H2Cr2O7;
②.根据表中各物质的溶度积常数可知,BaSO4与BaCrO4溶解度比较接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难与H2SO4接触,阻碍重铬酸生成;
(4).根据上述分析可知,沉淀BaCrO4进一步回收重铬酸的效果与温度、浓度、溶液pH、硫酸浓度、沉淀颗粒等有关,受到溶液pH、温度、H2SO4浓度、BaCrO4颗粒大小等因素的影响。