题目内容
【题目】已知:![]() 是碳酸甲乙酯的工业生产原理。下图是投料比[
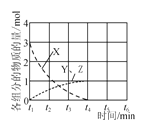
是碳酸甲乙酯的工业生产原理。下图是投料比[![]() ]分别为3:1和1:1、反应物的总物质的量相同时,
]分别为3:1和1:1、反应物的总物质的量相同时,![]() 的平衡转化率与温度的关系曲线。下列说法正确的是
的平衡转化率与温度的关系曲线。下列说法正确的是

A.曲线b所对应的投料比为3:1
B.M点对应的平衡常数小于Q点
C.N点对应的平衡混合气中碳酸甲乙酯的物质的量分数为0.58
D.M点和Q点对应的平衡混合气体的总物质的量之比为2:1
【答案】C
【解析】
试题分析:A.由图可知,温度一定时曲线b表示碳酸甲酯的转化率低,增大某一反应的浓度,其它反应物转化率增大,自身转化率降低,则曲线b表示所对应的投料比为1:1,A项错误;B. 根据图像可知,升高温度,碳酸甲酯的平衡转化率增大,说明平衡向正反应方向移动,K值增大,则M点对应的平衡常数大于Q点,B项错误;C.由A分析可知曲线b表示所对应的投料比为3:1,由图中数据可知,N点平衡时碳酸甲酯的转化率为58%,反应前后混合气体的总的物质的量不变,则平衡混合气中碳酸甲乙酯的物质的量分数为(1mol×0.58×2)÷(1mol+1mol)=0.58,C项正确;D.开始反应物的总物质的量相同,反应前后混合气体的总的物质的量不变,故曲线a、b平衡时混合气体的物质的量相等,D项错误;答案选C。

练习册系列答案
相关题目