题目内容
11.①1-丙醇 ②1,3-丙二醇 ③丙烷 ④乙醇 ⑤丙三醇等物质的沸点排列顺序正确的是( )| A. | ⑤>②>①>③>④ | B. | ⑤>④>③>②>① | C. | ⑤>②>①>④>③ | D. | ②>①>⑤>④>③ |
分析 醇的熔沸点高于烷烃,一元醇中碳原子个数越多其熔沸点越高,碳原子相同的醇中,醇羟基个数越多其熔沸点越高,据此分析解答.
解答 解:醇的熔沸点高于烷烃,所以丙烷的熔沸点最低;
一元醇中碳原子个数越多其熔沸点越高,所以熔沸点丙醇>乙醇;
碳原子相同的醇中,醇羟基个数越多其熔沸点越高,所以熔沸点丙三醇>1,3-丙二醇>1-丙醇,
通过以上分析知,这几种物质的熔沸点高低顺序是⑤>②>①>④>③,
故选C.
点评 本题考查物质熔沸点高低比较,因为氢键的存在导致碳原子个数相等的醇熔沸点高于烷烃,知道醇的熔沸点受碳原子个数、醇羟基个数影响,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列关于碱金属的描述正确的是( )
| A. | 碱金属都可以保存在煤油中 | |
| B. | 碱金属元素的单质硬度小、密度小、熔点低 | |
| C. | 在空气中加热均可生成多种氧化物 | |
| D. | 碱金属与水反应,均漂浮在水面上 |
2.在标准状况下,mgA气体与ngB气体分子数相等,下列说法不正确的是( )
| A. | 标准状况下,同体积的气体A、B质量比m:n | |
| B. | 25℃时,1Kg气体A与1Kg气体B的分子数之比为n:m | |
| C. | 同温同压下,气体A与气体B的密度之比为n:m | |
| D. | 标准状况下,等质量的A与B的体积比为n:m |
19.下列叙述中正确的是( )
| A. | 发生化学反应时,失去电子越多的金属原子,其还原能力越强 | |
| B. | 目前已发现118种元素,即已发现118种原子 | |
| C. | 核外电子总数相同的粒子,必定是同种元素的原子 | |
| D. | 同一元素的各种同位素的化学性质基本相同 |
6.据报道,${\;}_{67}^{166}$Ho可有效地治疗肝癌,该原子核内的中子数与核外电子数之差为( )
| A. | 32 | B. | 67 | C. | 99 | D. | 166 |
16.分子式为C4H10O的醇与C5H10O2的羧酸和浓H2SO4存在时共热生成的酯有( )
| A. | 4种 | B. | 8种 | C. | 12种 | D. | 16种 |
20.已知 和
和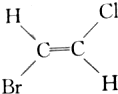 互为同分异构体(顺反异构),则化学式为C3H5Cl的链状化合物的同分异构体共有( )
互为同分异构体(顺反异构),则化学式为C3H5Cl的链状化合物的同分异构体共有( )
 和
和 互为同分异构体(顺反异构),则化学式为C3H5Cl的链状化合物的同分异构体共有( )
互为同分异构体(顺反异构),则化学式为C3H5Cl的链状化合物的同分异构体共有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
19.下列实验装置设计正确的是( )
| A. | 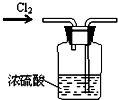 干燥氯气 | B. |  稀释浓硫酸 | ||
| C. |  实验室制氨气 | D. | 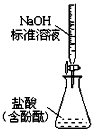 测定盐酸浓度 |
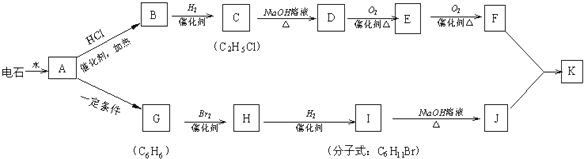
 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaBr;
+NaBr; .
.