题目内容
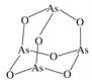
【题目】X、Y 、Z、W是原子序数依次增大的短周期主族元素,其中Z的最外层电子数与X的核外电子总数相等。X、Z、W形成的一种化合物结构为![]() ,该物质常用于制备纳米材料以及工业催化剂。下列说法正确的是
,该物质常用于制备纳米材料以及工业催化剂。下列说法正确的是
A.元素非金属性:X>Y>Z
B.简单离子半径:Y<Z< W
C.工业上常通过电解W与Z形成的化合物制备W单质
D.简单气态氢化物的稳定性:X<Z
【答案】D
【解析】
由化合物结构式可知X可以形成四个共价键,所以X为碳或硅,Z的最外层电子数与X的核外电子总数相等,所以Z为氧,X为碳,Y介于碳与氧之间,只能为氮,W显正二价,则W只能为镁。
A.同周期元素随原子序数递增,非金属性逐渐增强,所以元素非金属性:O>N>C,即Z>Y>X,故A项错误;
B.核外电子层数越多,半径越大,核外电子层数相同,核电荷数越小,半径越大,所以简单离子半径N3->O2->Mg2+,故B项错误;
C.MgO熔点高,工业上常通过电解氯化镁制得单质镁,故C错误;
D.非金属性越强,简单气态氢化物越稳定,所以CH4<H2O,故D正确;
故答案为D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目