��Ŀ����
����Ŀ���Ҵ��������������ҵ��������;�㷺����������¹����Ҵ��������������⣺
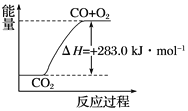
��1���Ҵ�����Ҫ��ȼ�ϣ���֪��25�桢101kPa�£�1kg�Ҵ����ȼ���ܷų�29713.04kJ������д����ʾ�Ҵ�ȼ���ȵ��Ȼ�ѧ����ʽ��_________________________________________��
��2���Ҵ�ȼ�ϵ��Ӧ��ǰ���ֹۣ���ϡ����Ϊ�������Һ��ȼ�ϵ�ص������缫��ӦʽΪ��__________���ڸ���������CO2�⣬�������˼����������ᣬд����������ĵ缫��Ӧʽ��_____________________________________��
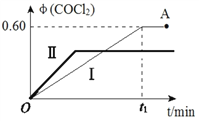
��3���Ҵ������ᷴӦ������������������Ӧ����ʽΪ��_______________________________�����ܱ������У����ø÷�Ӧ�Ʊ�����������ʵ��������ʼʱ�������м���3mol�Ҵ���1mol�����һ������Ũ���ᣬ��ַ�Ӧ�������в������Ҵ�����Ϊ______________��
A��2mol B��2.6mol C��2.8mol D��3mol
��4����Ӧ�����Ӧ������м���_____________��Һ�����÷�Һ©�����������������
���𰸡�C2H5OH(l)+3O2(g)=2CO2+3H2O(l) ��H=-1366.8kJ/molO2+4e-+4H+=2H2OCH3CH2OH -4e- +H2O = CH3COOH + 4H+CH3COOH+CH3CH2OH![]() CH3COOCH2CH3 + H2OBCNa2CO3
CH3COOCH2CH3 + H2OBCNa2CO3
��������
���⿼������Ȼ�ѧ����ʽ��ȼ�ϵ�صĵ��ӷ�Ӧ����д�Լ�������Ӧ����д�ͼ��㣬ע��ȼ���ȵĶ��塣
(1)ȼ����ָ1mol��ȼ����ȫȼ�������ȶ���������ʱ�ų�������������Ҫ����1mol�Ҵ���Ӧʱ��������1kg�Ҵ������ʵ���Ϊ1000/46mol����1mol�Ҵ�ȼ�շų�������Ϊ![]() kJ�����Ҵ�ȼ���ȵ��Ȼ�ѧ����ʽΪ��C2H5OH(l)+3O2(g)=2CO2+3H2O(l) ��H=-1366.8kJ/mol��(2)�Ҵ�ȼ�ϵ����������������Ӧ����Ϊ��ҺΪ���ԣ������õ����ӽ������������ˮ���缫��ӦΪ��O2+4e-+4H+=2H2O���Ҵ�ʧȥ�����������ᣬ�缫��ӦΪ��CH3CH2OH -4e- +H2O = CH3COOH + 4H+��(3)������Ҵ���Ӧ��������������ˮ������ʽΪ��CH3COOH+CH3CH2OH
kJ�����Ҵ�ȼ���ȵ��Ȼ�ѧ����ʽΪ��C2H5OH(l)+3O2(g)=2CO2+3H2O(l) ��H=-1366.8kJ/mol��(2)�Ҵ�ȼ�ϵ����������������Ӧ����Ϊ��ҺΪ���ԣ������õ����ӽ������������ˮ���缫��ӦΪ��O2+4e-+4H+=2H2O���Ҵ�ʧȥ�����������ᣬ�缫��ӦΪ��CH3CH2OH -4e- +H2O = CH3COOH + 4H+��(3)������Ҵ���Ӧ��������������ˮ������ʽΪ��CH3COOH+CH3CH2OH![]() CH3COOCH2CH3 + H2O����Ϊ������Ӧ�ǿ��淴Ӧ�����Է�Ӧ�ﲻ����ȫ��Ӧ������1mol������ȫ��Ӧ����1mol�Ҵ������Բ������Ҵ������ʵ���Ӧ��2mol-3mol����ѡBC��(6)��Ӧ��Ļ������������������������Ҵ������Լ���̼���ƽ��з��룬̼������Һ���ܽ��Ҵ�����Ӧ���ᣬ���������������ܽ�ȡ�
CH3COOCH2CH3 + H2O����Ϊ������Ӧ�ǿ��淴Ӧ�����Է�Ӧ�ﲻ����ȫ��Ӧ������1mol������ȫ��Ӧ����1mol�Ҵ������Բ������Ҵ������ʵ���Ӧ��2mol-3mol����ѡBC��(6)��Ӧ��Ļ������������������������Ҵ������Լ���̼���ƽ��з��룬̼������Һ���ܽ��Ҵ�����Ӧ���ᣬ���������������ܽ�ȡ�

 ��������ϵ�д�
��������ϵ�д�����Ŀ����֪������Ũ��Ϊ0.lmol/L��������Һ��pH���±��������й�˵����ȷ����
���� | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
A. ����ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳�� H2CO3<HClO<HF
B. �����ϱ���ˮ�ⷽ��ʽClO-+H2O![]() HClO+OH-��ˮ�ⳣ��K=10-7.6
HClO+OH-��ˮ�ⳣ��K=10-7.6
C. ����CO2ͨ��0.lmol/LNa2C03��Һ������Һ���ԣ�����Һ��2c(CO32-)+c(HCO3-)=0.1 mol/L
D. ������NaC1O��Һ��ͨHF������ǡ����ȫ��Ӧʱ��c(Na+)>c(F-)>(H+)>c(HClO)>c(OH-)