题目内容
氯是重要的非金属元素。
30.NaCl和浓硫酸微热制取氯化氢的化学方程式为 ;
可用 试纸放在瓶口以检验氯化氢气体是否集满。
31.新制氯水中含有的分子有:Cl2、H2O和 ;光照新制氯水的化学方程式为 ;工业是用电解食盐水制取氯气,阴极的电极反应式为:
2H++2e→H2↑,则阳极的电极反应式为 。
32.已知还原性SO32->I->Br-.向NaBr、NaI、Na2SO3混合溶液中,通入—定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是______(选填编号)。
a. NaCl Na2SO4 b. NaCl NaBr Na2SO4
c. NaCl Na2SO4 I2 d. NaCl NaI Na2SO4
30.NaCl+ H2SO4 (浓)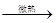 NaHSO4+HCl↑(2分);湿的蓝色石蕊试纸(或湿的pH试纸)(1分)。
NaHSO4+HCl↑(2分);湿的蓝色石蕊试纸(或湿的pH试纸)(1分)。
31.HClO(1分); 2 HClO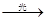 2HCl+O2↑(1分); 2Cl--2e→Cl2↑(1分)
2HCl+O2↑(1分); 2Cl--2e→Cl2↑(1分)
32.ab(2分)
解析试题分析:30.NaCl和浓硫酸微热制取氯化氢时生成NaHSO4;氯化氢气体为酸性气体,可用湿润的紫色石蕊试纸等放在瓶口以检验氯化氢气体是否集满。
31.新制氯水中含有的分子有:Cl2、H2O和HClO;光照新制氯水,氯水中的HClO分解为HCl和O2;工业是用电解食盐水制取氯气,阴极是阳离子H+放电生成H2,2H++2e→H2↑,阳极是阴离子Cl-放电生成Cl2。
32.已知还原性SO32->I->Br-.向NaBr、NaI、Na2SO3混合溶液中,通入—定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是
极少Cl2:只有Na2SO3部分反应,产物NaCl、NaBr、NaI、Na2SO4(由Na2SO3在空气中氧化),b正确。;
适量Cl2:有NaI、Na2SO3反应,产物NaCl、NaBr、Na2SO4;
过量Cl2:NaBr、NaI、Na2SO3全分反应,产物NaCl、Na2SO4,a正确 。
考点:Cl的单质及其化合物的性质,还原性强弱与反应的顺序。

 阅读快车系列答案
阅读快车系列答案某固体粉末中可能含有KNO3、Cu(NO3)2、AgNO3三种物质中的一种或多种,取一定量该固体粉末,加热后得到A气体a L,将气体用足量水吸收,剩余气体B的体积为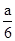 L。下列相关推测错误的是
L。下列相关推测错误的是
| A.气体B可能是O2,也可能是NO |
| B.固体粉末的组成为n(KNO3):n(Cu(NO3)2):n(AgNO3)=1:1:3 |
| C.固体粉末的组成为n(KNO3):n(Cu(NO3)2):n(AgNO3)=1:1:1 |
| D.气体A 中NO2与O2的体积比为9:1 |
稀硫酸中插一块铜片,加入下列物质后,可使铜片发生反应的是 ( )
| A.稀盐酸 | B.硫酸钠晶体 | C.硝酸钾晶体 | D.氯化钠晶体 |
近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)火力发电厂为除去有害气体SO2,并变废为宝,常采用尾气脱硫工艺,如图所示。写出尾气脱硫工艺中反应的化学方程式: 。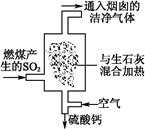
(2)宁波的火力发电厂通常建在海边,一般海水呈弱碱性,主要含有Na+、Mg2+、K+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子。含有SO2的烟气也可以利用海水脱硫,其工艺流程如下图所示: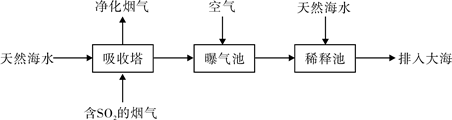
①向曝气池通入空气的目的是 。
②通入空气后的曝气池中的海水与天然海水相比,浓度有明显不同的离子是 。
| A.Cl- | B.Na+ | C.Mg2+ | D.HCO3- |
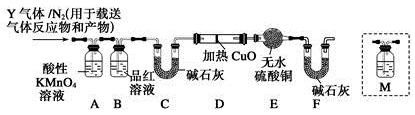
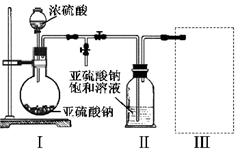

 H++Cl-+ HClO,其平衡常数表达式为K= 。
H++Cl-+ HClO,其平衡常数表达式为K= 。