题目内容
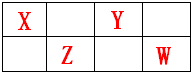 如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,Z元素原子最外层电子数与电子总数之比为1:3.下列说法正确的是( )
如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,Z元素原子最外层电子数与电子总数之比为1:3.下列说法正确的是( )A、X的最简单气态氢化物的球棍模型为: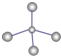 |
| B、原子半径由大到小的顺序为:W>Z>Y>X |
| C、X、Y、Z、W元素都能形成两种同素异形体 |
| D、X与Y、Z与W都能化合形成两种化合物 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W均为短周期元素,根据元素在周期表中位置可知,X、Y处于第二周期,Z、W处于第三周期,Z元素原子最外层电子数与电子总数之比为1:3,设Z的最外层电子数是x,则x:(x+10)=1:3,x=5,所以Z是P元素,则W是Cl元素,X是C元素,Y是O元素,据此解答.
解答:
解:X、Y、Z、W均为短周期元素,根据元素在周期表中位置可知,X、Y处于第二周期,Z、W处于第三周期,Z元素原子最外层电子数与电子总数之比为1:3,设Z的最外层电子数是x,则x:(x+10)=1:3,x=5,所以Z是P元素,则W是Cl元素,X是C元素,Y是O元素,
A.X的最简单气态氢化物为CH4,C原子半径大于H原子半径,而球棍模型之间H原子半径大于碳原子半径,不符合实际,故A错误;
B.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径由大到小的顺序为:Z>W>X>Y,故B错误;
C.碳元素单质存在金刚石、石墨、C60等多种同素异形体,氯气不存在同素异形体,故C错误;
D.C与O可以形成CO、CO2,P与Cl可以形成PCl3、PCl5,故D正确,
故选D.
A.X的最简单气态氢化物为CH4,C原子半径大于H原子半径,而球棍模型之间H原子半径大于碳原子半径,不符合实际,故A错误;
B.同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径由大到小的顺序为:Z>W>X>Y,故B错误;
C.碳元素单质存在金刚石、石墨、C60等多种同素异形体,氯气不存在同素异形体,故C错误;
D.C与O可以形成CO、CO2,P与Cl可以形成PCl3、PCl5,故D正确,
故选D.
点评:本题考查原子结构和元素周期律的关系,正确推断元素是解本题关键,难度不大,A选项为易错点,学生容易考虑空间结构而忽略原子半径大小.

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、5.6g铁和6.4g铜分别与0.1mol氯气完全反应,转移的电子数相等 |
| B、0.5mol O3与11.2L O2所含的分子数一定相等 |
| C、等质量的14NO和13CO气体中含有的中子数相等 |
| D、常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
下列反应属于取代反应的是( )
A、CH2=CH2+H2O
| |||
B、2CH3CH2OH+O2
| |||
C、nCH2=CH2
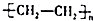 | |||
D、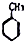 +3HNO3 +3HNO3
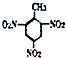 +3H2O +3H2O |
绿原酸是咖啡的热水提取液成分之一,结构简式如图,关于绿原酸判断正确的是( )
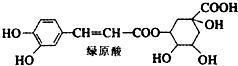

| A、绿原酸能使酸性KMnO4溶液褪色 |
| B、绿原酸水解产物均可以与FeCl3溶液发生显色反应 |
| C、1mol绿原酸与足量溴水反应,最多消耗2.5mol Br2 |
| D、1mol绿原酸与足量NaOH溶液反应,最多消耗8mol NaOH |
已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系,A
B
C
D且D为强电解质(其它相关物质可能省略)下列说法不正确的是( )
| O2 |
| O2 |
| H2O |
| A、若A为非金属单质,则它与Mg反应的产物,其阴阳离子个数比可能为2:3 |
| B、若A为非金属单质,则其元素在周期表中的位置可能处于第二周期第IVA族 |
| C、不论A为单质还是化合物,D都有可能是同一种物质,该物质的浓溶液在常温下都能使铁和铝发生钝化 |
| D、若A是共价化合物,O.1mol的A分子中含有的电子数可能为NA(NA为阿佛加德罗常数的值) |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol-1,则氢气的燃烧热为241.8 kJ?mol-1 |
| B、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 |
| C、已知2C(s)+2O2(g)═2CO2(g)△H=a;2C(s)+O2(g)═2CO(g)△H=b,则a>b |
| D、已知C(石墨,s)═C(金刚石,s)△H>0,则石墨比金刚石稳定 |