题目内容
7.n摩某金属R与足量盐酸反应,生成RClx和标准状况下V升氢气,则x值为( )| A. | 11.2nV | B. | $\frac{V}{11.2n}$ | C. | 22.4nV | D. | $\frac{n}{22.4V}$ |
分析 金属与盐酸反应方程式为:R+xHCl=RClx+$\frac{x}{2}$H2↑,由方程式可知1molR与盐酸完全反应生成标况下11.2xL的氢气,而n摩某金属R与足量盐酸反应,生成标准状况下V升氢气,则两者成比例列出关系式解答.
解答 解:金属与盐酸反应方程式为:R+xHCl=RClx+$\frac{x}{2}$H2↑,由方程式可知1molR与盐酸完全反应生成标况下11.2xL的氢气,而n摩某金属R与足量盐酸反应,生成标准状况下V升氢气,所以$\frac{1}{n}=\frac{11.2x}{V}$,解之得x=$\frac{V}{11.2n}$,故选:B.
点评 本题考查物质的量的相关计算,为高频考点,题目难度不大,本题注意相关物质的量的相关计算公式的运用,把握物质的量应用于化学方程式的计算.

练习册系列答案
相关题目
17.向某溶液中滴加KSCN 溶液,无明显现象,再向其中滴加氯水,溶液变为血红色,则下列说法正确的是
( )
( )
| A. | 原溶液中一定含有Fe3+离子,不含Fe2+ | |
| B. | 原溶液中一定含有Fe2+离子,不含Fe3+ | |
| C. | 溶液中的Fe2+离子被氯气还原为Fe3+ | |
| D. | 溶液中同时含Fe2+或Fe3+离子 |
18.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L乙醇所含的分子数为NA | |
| B. | 1mol/LCaCl2溶液中含有的氯离子数目为2NA | |
| C. | 1 mol金属钠在足量氧气中完全燃烧转移的电子数为2NA | |
| D. | 28g N2中含有的原子数为2NA |
15.下列实验操作,现象和结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 稀硫酸滴入碳酸钠溶液中,将产生的气体通入盛有硅酸钠溶液的烧杯中 | 烧杯中产生白色胶状沉淀 | 非金属性:S>C>Si |
| B | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 该溶液一定是钠盐溶液 |
| C | 将饱和氯化铁溶液滴入盛有沸水的烧杯中,继续煮沸至溶液呈红褐色,停止加热,用激光笔照射烧杯中的液体 | 看到一条光亮的“通路” | 证明生成了氢氧化铁沉淀 |
| D | 在分液漏斗中加入碘水后再加入CCl4,充分振荡、静置 | 分层,且上层溶液呈紫色 | CCl4可作为碘的萃取剂 |
| A. | A | B. | B | C. | C | D. | D |
12.A元素原子的M层有3个电子,B元素原子的L层有6个电子,则A,B两元素形成的化合物的化学式式量为( )
| A. | 59 | B. | 102 | C. | 114 | D. | 150 |
7.对于放热反应,下列说法中正确的是( )
| A. | 反应物的总能量一定低于生成物的总能量 | |
| B. | 所有的中和反应都为放热反应 | |
| C. | 破坏反应物中的化学键所吸收的总能量大于形成生成物中化学键所放出的总能量 | |
| D. | 放热反应,不必加热就可发生 |
5.用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
| A. | 对反应体系加热 | B. | 改用体积大的反应容器 | ||
| C. | 加入少量硫酸铜溶液 | D. | 改用铁粉代替铁片 |
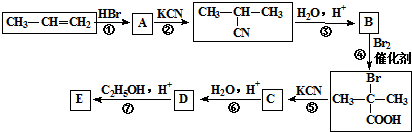
 .
.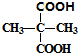 +2C2H5OH$→_{△}^{浓硫酸}$
+2C2H5OH$→_{△}^{浓硫酸}$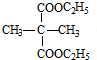 +2H2O.
+2H2O.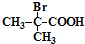 与足量NaOH水溶液反应的化学方程式为
与足量NaOH水溶液反应的化学方程式为 .
.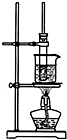 1834年,德国科学家米希尔里希通过蒸馏苯甲酸和石灰的混合物,得到了鱼法拉第所制液体相同的一种液体,并命名为苯.后来,法国化学家热拉尔等人又确定了苯的分子式为C6H6.
1834年,德国科学家米希尔里希通过蒸馏苯甲酸和石灰的混合物,得到了鱼法拉第所制液体相同的一种液体,并命名为苯.后来,法国化学家热拉尔等人又确定了苯的分子式为C6H6.