题目内容
18.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,22.4L乙醇所含的分子数为NA | |
| B. | 1mol/LCaCl2溶液中含有的氯离子数目为2NA | |
| C. | 1 mol金属钠在足量氧气中完全燃烧转移的电子数为2NA | |
| D. | 28g N2中含有的原子数为2NA |
分析 A.气体摩尔体积适用对象为气体;
B.溶液体积未知;
C.钠与氧气反应无论生成氧化钠还是过氧化钠,钠都是+1价;
D.质量转化为物质的量,结合氮气分子的构成解答.
解答 解:A.标况下,乙醇为液体,不能使用气体摩尔体积,故A错误;
B.溶液体积未知,无法计算氯离子的物质的量和个数,故B错误;
C.钠与氧气反应无论生成氧化钠还是过氧化钠,钠都是+1价,所以1 mol金属钠在足量氧气中完全燃烧转移的电子数为NA,故C错误;
D.28g N2中含有的原子数=$\frac{28g}{28g/mol}$×2×NA=2NA,故D正确;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子所含原子数目是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列各组物质的性质中不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 热稳定性:H2S>H2O>HF | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 氧化性:F2>Cl2>Br2 |
9.硒(Se)是人体必需的微量元素,它的一种同位素是${\;}_{34}^{80}$Se.下列有关该同位素的说法止确的是( )
| A. | 质子数为80 | B. | 中子数为46 | C. | 电子数为114 | D. | 质量数为34 |
13.下列物质①Na2CO3②Al③Al2O3④Al(OH)3中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
| A. | ③④ | B. | ②③④ | C. | ②③ | D. | 全部 |
3.A、B、C、D、E五种短周期元素,其原子序数逐渐增大,元素A的单质是密度最小的气体,元素B的单质存在两种以上同位素异形体,且其中一种是自然界中硬度最大的单质,元素D的最外层电子数是次外层电子数的三倍,B、C、D、E四种元素均能与A形成等电子数的四种分子,且化合物中各原子的个数比如表
下列说法正确的是( )
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 原子个数比 | B:A=1:3 | C:A=1:2 | D:A=1:1 | E:A=1:1 |
| A. | 元素E在元素周期表中的位置为第三周期、VIIA族 | |
| B. | 原子半径:A<B<C<D | |
| C. | 甲和丙分子均只含极性键 | |
| D. | A、B、C、D四种元素中的三种能形成多种与甲分子等电子数的化合物 |
10.下列各组中的两种有机物一定互为同系物的是( )
| A. | CH4O和C2H6O | B. | C2H4和C6H12 | C. | C2H2和C4H6 | D. | CH4和C3H8 |
7.n摩某金属R与足量盐酸反应,生成RClx和标准状况下V升氢气,则x值为( )
| A. | 11.2nV | B. | $\frac{V}{11.2n}$ | C. | 22.4nV | D. | $\frac{n}{22.4V}$ |
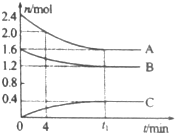 T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示. 能源与材料、信息一起被称为现代社会发展的三大支柱,现代社会的一切活动都离不开能源,能源的利用与相互转化始终与我们息息相关.
能源与材料、信息一起被称为现代社会发展的三大支柱,现代社会的一切活动都离不开能源,能源的利用与相互转化始终与我们息息相关.