题目内容
17.向某溶液中滴加KSCN 溶液,无明显现象,再向其中滴加氯水,溶液变为血红色,则下列说法正确的是( )
| A. | 原溶液中一定含有Fe3+离子,不含Fe2+ | |
| B. | 原溶液中一定含有Fe2+离子,不含Fe3+ | |
| C. | 溶液中的Fe2+离子被氯气还原为Fe3+ | |
| D. | 溶液中同时含Fe2+或Fe3+离子 |
分析 铁离子检验方法:溶液中加入硫氰酸钾溶液,溶液变为血红色,证明是含有三价铁离子;
亚铁离子检验方法:液中加入KSCN溶液无明显现象,再滴加氯水,溶液立即变为血红色,说明原溶液含有亚铁离子,加入氯水发生反应为:2Fe2++Cl2=2Fe3++2Cl-,生成的铁离子和硫氰酸根离子生成血红色溶液.
解答 解:液中加入KSCN溶液无明显现象,再滴加氯水,溶液立即变为血红色,说明原溶液含有亚铁离子,
A、原溶液滴加KSCN的溶液,无明显现象,说明一定没有铁离子,再向其中滴加氯水,溶液变为血红色,说明溶液中一定存在亚铁离子,故A错误;
B、根据以上分析可知,原溶液中一定含有Fe2+离子,不含Fe3+,故B正确;
C、溶液中的亚铁离子被氯气氧化为铁离子,故C错误;
D、滴加KSCN的溶液,无明显现象,说明原溶液中一定没有铁离子,故D错误;
故选B.
点评 本题考查了铁离子、亚铁离子的检验方法,题目难度不大,要求学生掌握铁离子、亚铁离子的检验方法,掌握二价铁离子和三价铁离子之间的转化关系.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
8.下列各组物质的性质中不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 热稳定性:H2S>H2O>HF | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 氧化性:F2>Cl2>Br2 |
5.X、Y、Z、W、R是短周期元素,X原子的电子总数等于其电子层数的3倍,Y元素在地壳中的含量很多,Z+、W2+、与Y2-具有相同的电子层结构,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述正确的是( )
| A. | 元素Z、W分别与Y形成的常见化合物均为碱性氧化物 | |
| B. | X和R形成的常见化合物中各原子都达到8电子稳定结构 | |
| C. | 离子半径的大小顺序为:Z+>W2+>Y2- | |
| D. | 含有Y、Z、R三种元素的化合物最多只有3种 |
12.为了实现下列实验目的,依据下表提供的主要仪器,所用的试剂合理的是( )
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 测定氨水的浓度 | 锥形瓶、滴定管、烧杯 | 氨水、1mol/L盐酸、甲基橙 |
| B | 制备Fe(OH)3胶体 | 烧杯、胶头滴管、酒精灯 | 饱和FeCl3溶液、NaOH溶液 |
| C | 检验丙烯醛中的碳碳双键 | 试管、胶头滴管 | 丙烯醛、溴水 |
| D | 配制100mL1mol/L硫酸 | 容量瓶、胶头滴管、10mL量筒、烧杯 | 18mol/L硫酸、蒸馏水 |
| A. | A | B. | B | C. | C | D. | D |
9.硒(Se)是人体必需的微量元素,它的一种同位素是${\;}_{34}^{80}$Se.下列有关该同位素的说法止确的是( )
| A. | 质子数为80 | B. | 中子数为46 | C. | 电子数为114 | D. | 质量数为34 |
7.n摩某金属R与足量盐酸反应,生成RClx和标准状况下V升氢气,则x值为( )
| A. | 11.2nV | B. | $\frac{V}{11.2n}$ | C. | 22.4nV | D. | $\frac{n}{22.4V}$ |
 .
.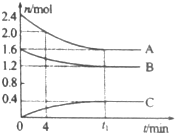 T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.