��Ŀ����
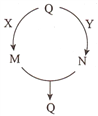
����Ŀ����ͼ��ʾװ�ÿɼ��������ҵ��ˮ�к������ӣ�NH4+��������˵������ȷ����

A. ���ǵ���ת��Ϊ��ѧ�ܵ�װ��
B. ������������ʱ�����ӷ���ʽΪ��3Cl2 + 2NH4+=N2 + 6Cl-+8H+
C. ������H2��N2�����ʵ���֮��Ϊ3:1���������ˮ��pH��С
D. ��ع���ʱ���׳��е�Na������Mg�缫
���𰸡�D
��������A�����л��ý���þ��ԭ��صĸ�����ʯīΪ�����γ�ԭ��أ���������ԭ��صĵ��أ�������Թ�ҵ��ˮ�������ǽ�����ת��Ϊ��ѧ�ܵ�װ�ã�ѡ��A��ȷ��B�����������º�����������ʱת��Ϊ��������Ӧ�����ӷ���ʽΪ��3Cl2 + 2NH4+=N2 + 6Cl-+8H+��ѡ��B��ȷ��C��������H2��N2�����ʵ���֮��Ϊ3:1�����ݵ缫��Ӧ6H++6e-=3H2����3Cl2 + 2NH4+=N2 + 6Cl-+8H+���������ˮ��H+Ũ������pH��С��ѡ��C��ȷ��D����ع���ʱ���׳���ԭ��أ�ԭ�����������Na����������ʯī�缫��ѡ��D����ȷ����ѡD��
�����͡���ѡ��
��������
7
����Ŀ����֪ij���������Һ�п��ܺ���NO3- ��Cl- ��SO42-��CO32-��NH4+��Fe3+��Al3+��K+�еļ��֣������������ӵ����ʵ�����ȡ�Ϊȷ������Һ�ijɷ֣�ijѧϰС����������ʵ�飺��ȡ����Һ100mL���������NaOH��Һ�����ȵõ�0.02mol���壬ͬʱ�������ɫ������ �ڽ��������ˡ�ϴ�ӡ����գ��õ�1.6 g���壻 ����������Һ�м�������BaCl2��Һ���õ�4.66 g����������ij���������˵����ȷ����
A. ����ȷ��ԭ��Һ���Ƿ���Al3+��K+
B. ԭ��Һ�к��е�����ֻ�У�Cl- ��SO42-��NH4+��Fe3+
C. ԭ��Һ��c(NO3-)��0.2 mol��L-1 c(Fe3+)=0.2 mol��L-1
D. ��ԭ��Һ�м�������������������Һ�����������������������
���𰸡�C
����������ȡ����Һ100mL���������NaOH��Һ�����ȵõ�0.02mol���壬˵����Һ�к���0.02mol NH4+��ͬʱ�������ɫ����Ϊ����������˵����Һ�к���Fe3+��CO32-��Fe3+�ᷢ��˫ˮ������ܴ������棬����Һ��һ������CO32-���ڽ��������ˡ�ϴ�ӡ����գ��õ�1.6 g����Ϊ����������n[Fe(OH)3]=2n(Fe2O3)=2��![]() =0.02mol�� ����������Һ�м�������BaCl2��Һ���õ�4.66 g����������ij����������Ϊ���ᱵ��n��SO42-��=n(BaSO4)=
=0.02mol�� ����������Һ�м�������BaCl2��Һ���õ�4.66 g����������ij����������Ϊ���ᱵ��n��SO42-��=n(BaSO4)= ![]() =0.02mol��n(+)=n(NH4+)+3n(Fe3+)=0.02mol+3��0.02mol=0.08mol��n(-)=2 n��SO42-��=2��0.02mol=0.04mol<0.08mol������Һ�л������������ӣ������������ӵ����ʵ�����ȣ���n(-)=2 n��SO42-��+n(NO3-)+n(Cl-)=2��0.02mol+0.02mol+0.02mol=0.08mol�������Һ��һ������NO3- ��Cl-��һ������Al3+��K+����A.ԭ��Һ��һ������Al3+��K+��ѡ��A����B. ԭ��Һ�к��е�����ֻ�У�NO3- ��Cl- ��SO42-��NH4+��Fe3+��ѡ��B����C. ԭ��Һ��c(NO3-)��0.2 mol��L-1��c(Fe3+)=0.2 mol��L-1��ѡ��C��ȷ��D. ��ԭ��Һ�м������������ۣ�������Ӧ��2Fe3++ Fe = 3Fe2+������Һ��������������������������䣬ѡ��D����ѡC��
=0.02mol��n(+)=n(NH4+)+3n(Fe3+)=0.02mol+3��0.02mol=0.08mol��n(-)=2 n��SO42-��=2��0.02mol=0.04mol<0.08mol������Һ�л������������ӣ������������ӵ����ʵ�����ȣ���n(-)=2 n��SO42-��+n(NO3-)+n(Cl-)=2��0.02mol+0.02mol+0.02mol=0.08mol�������Һ��һ������NO3- ��Cl-��һ������Al3+��K+����A.ԭ��Һ��һ������Al3+��K+��ѡ��A����B. ԭ��Һ�к��е�����ֻ�У�NO3- ��Cl- ��SO42-��NH4+��Fe3+��ѡ��B����C. ԭ��Һ��c(NO3-)��0.2 mol��L-1��c(Fe3+)=0.2 mol��L-1��ѡ��C��ȷ��D. ��ԭ��Һ�м������������ۣ�������Ӧ��2Fe3++ Fe = 3Fe2+������Һ��������������������������䣬ѡ��D����ѡC��

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д� ѧҵ����һ��һ��ϵ�д�
ѧҵ����һ��һ��ϵ�д�����Ŀ����ҵ���Ʊ�H2��һ����Ҫ�����ǣ�CO��g��+H2O��g��CO2 ��g��+H2��g����H=QkJ/mol����֪�÷�Ӧ��ƽ�ⳣ��K���¶�T�Ĺ�ϵ��ͼ��ʾ������һ�̶��ݻ����ܱ������У�850��ʱ����������Ӧ����������ڸ����ʵ�Ũ�� ��mol/L����ʱ��ı仯��ϵ�������֪��850��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=1.0����ش��������⣺
ʱ��/min | CO��g�� | H2O��g�� | CO2��g�� | H2��g�� |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |

��1��Q0�����������=����������
��2������850��ʱ��Ӧ�����г���H2O��g����Kֵ�����������С�����䡱����
��3���ϱ��� c2Ϊmol/L��CO��g����ת����Ϊ ��