题目内容
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同. 
回答下列问题:
(1)B的元素名称为 , D在周期表中的位置 .
(2)A,C,D对应的离子半径由大到小顺序为 , (用化学符号表示)
(3)D的单质与水反应的离子方程式为 .
(4)向D与E形成的化合物的水溶液中滴入过量烧碱溶液,用离子方程式表述 .
【答案】
(1)磷;第三周期ⅦA族
(2)S2﹣>Cl﹣>O2﹣
(3)Cl2+H2O=H++Cl﹣+HClO
(4)Al3++4OH﹣=AlO2﹣+2H2O
【解析】解:由短周期及元素在周期表的位置,设C的质子数为x,B的为x﹣1,D的为x+1,A的为x﹣8, 由A、B、C、D四种元素原子核外共有56个电子,则
x+(x﹣1)+(x+1)+(x﹣8)=56,解得x=16,
即C为硫,B为磷,D为氯,A为氧;
又1molE单质与足量酸作用,在标准状况下能产生33.6LH2 , 设E的化合价为y,
由电子守恒可知,1mol×(y﹣0)= ![]() ×2×(1﹣0),
×2×(1﹣0),
解得y=+3,且E的阳离子与A的阴离子核外电子层结构完全相同,即E的质子数为10+3=13,则E为铝;(1)B为磷,D为氯,Cl原子有3个电子层,最外层电子数为7,则在第三周期ⅦA族,所以答案是:磷;第三周期ⅦA族;(2)根据电子层数越多,半径越大,具有相同结构的离子,原子序数越小的离子半径越大,则离子半径为S2﹣>Cl﹣>O2﹣ , 所以答案是:S2﹣>Cl﹣>O2﹣;(3)氯气和水反应生成盐酸和次氯酸,离子反应中气体、水、次氯酸应保留化学式,则离子反应为Cl2+H2O=H++Cl﹣+HClO,所以答案是:Cl2+H2O=H++Cl﹣+HClO;(4)D和E形成的化合物为AlCl3 , 水溶液中滴入过量烧碱溶液生成偏铝酸钠和水,离子反应为Al3++4OH﹣﹣=AlO2﹣+2H2O,所以答案是:Al3++4OH﹣﹣=AlO2﹣+2H2O.

 名校课堂系列答案
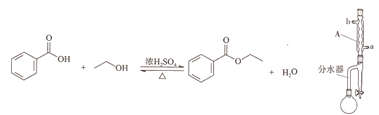
名校课堂系列答案【题目】实验室制备苯甲酸乙酯的反应装置示意图和有关数据如下:
相对分子质量 | 密度/(g/cm3) | 沸点/℃ | 水中溶解性 | |
苯甲酸 | 122 | 1.266 | 249 | 微溶 |
乙醇 | 46 | 0.789 | 78.3 | 溶 |
苯甲酸乙酯 | 150 | 1.045 | 213 | 难溶 |
环己烷 | 84 | 0.779 | 80.8 | 难溶 |
环已烷、乙醇和水可形成共沸物,其混合物沸点为62.1℃。
合成反应:向圆底烧瓶中加入6.1g苯甲酸、20mL无水乙醇、25mL环已烷和2片碎瓷片,搅拌后再加入2mL浓硫酸。按图组装好仪器后,水裕加热回流1.5小时。
分离提纯:继续水浴加热蒸出多余乙醇和环已烷,经分水器放出。剩余物质倒入盛有60mL冷水的烧怀中,依次用碳酸钠、无水氯化钙处理后,再蒸馏纯化,收集210~213℃的馏分。得产品5.0g。
回答下列问题:
(1)仪器A的名称为_______,冷却水应从______(填“a”或“b”)口流出。
(2)加入环己烷的目的为______________。
(3)合成反应中,分水器中会出现分层现象,且下层液体逐渐增多,当下层液体高度超过距分水器支管约2cm时开启活塞放出少量下层波体。该操作的目的为_________________。
(4)实验中加入碳酸钠的目的为__________;经碳酸钠处理后,若粗产品与水分层不清,可采取的措施为___________(填字母)。
(5)在该实验中,圆底烧瓶的容积最适合的是_____。
A.50mL B.100mL C.200mL D.300mL
(6)本实验的产率为______________。
【题目】某化学兴趣小组为了探究碳酸钙与稀盐酸反应过程中的速率变化,在VmL稀盐酸中加入足量的碳酸钙,收集反应放出的CO2(气体体积已换算为标准状况下的数值),实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
CO2体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)0~1 min、1~2 min、2~3 min、3~4 min、4~5 min五个时间段中,_________反应速率最快。
(2)假设溶液体积不变,4~5min时间段以盐酸的浓度变化来表示的该反应速率为____________________________。
(3)为了降低上述化学反应的反应速率,向溶液中加入下列物质,你认为可行的是
_______________(填编号)。
a.蒸馏水 b.浓盐酸 c.NaCl固体 d.NaCl溶液
(4)除了上述方法外,你认为还可以采取哪些措施来降低化学反应速率?(试写两条)_______________________________________________________________________,
________________________________________________________________________。