题目内容
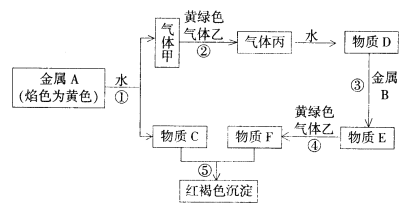
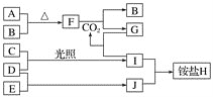
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
【答案】N2 NH3 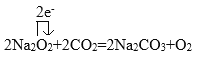 Cl2+2I-=I2+2Cl- 0.3NA
Cl2+2I-=I2+2Cl- 0.3NA
【解析】
化合物G的焰色反应为黄色,含有Na元素,F能与二氧化碳反应得到气体单质B与G,可推知F为Na2O2,B为O2,G为Na2CO3,而A与B(氧气)反应得到F(过氧化钠),则A为Na。G(Na2CO3)与I反应得到CO2,则I属于酸,I由气体非金属单质C与D在光照条件下得到,则I为HCl,C、D分别为H2、Cl2中的一种,I和J通常状况下呈气态,二者反应得到铵盐,且D和E反应生成一种刺激性气味的气体,可推知D为H2,C是Cl2,E为N2,J为NH3,铵盐为NH4Cl,据此解答。
根据上述分析可知:A是Na,B是O2,C是Cl2,D是H2,E是N2,F是Na2O2,G是Na2CO3,铵盐H为NH4Cl,I为HCl,J是NH3。
(1)E是N2,J是NH3;
(2)F是Na2O2,Na2O2和CO2反应产生碳酸钠和氧气,该反应的方程式为:2Na2O2+2CO2=2Na2CO3+O2,用单线桥法表示电子转移的情况: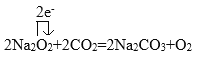 ;
;
(3)Cl2具有氧化性,将少量单质Cl2通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,说明发生置换反应生成I2单质,该反应的离子方程式为:Cl2+2I-=I2+2Cl-;
(4)A和B反应方程式为:2Na+O2![]() Na2O2,参加反应氧气的物质的量n(O2)=
Na2O2,参加反应氧气的物质的量n(O2)=![]() =0.15mol,在反应中氧元素由0价降低为-1价,则反应过程转移电子的数目为N(e-)=0.15mol×2×NA/mol=0.3NA。
=0.15mol,在反应中氧元素由0价降低为-1价,则反应过程转移电子的数目为N(e-)=0.15mol×2×NA/mol=0.3NA。

 阅读快车系列答案
阅读快车系列答案