题目内容
20.下列离子方程式不正确的是( )| A. | 用碳酸钠溶液吸收少量二氧化硫:2 CO32-+SO2+H2O=2 HCO3-+SO32- | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液使SO42-沉淀完全:2Ba2++NH4++Al3++2 SO42-+4OH-=Al(OH)3↓+2BaSO4↓+NH3•H2O | |
| C. | 0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合:HSO3-+ClO-=SO42-+Cl-+H+ | |
| D. | 将1 mol/L NaAlO2溶液和1.5 mol/L HCl溶液等体积互相均匀混合:6 AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
分析 A.二氧化硫少量反应生成碳酸氢钠和亚硫酸钠;
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,说明SO42-与Ba2+的比例是1:2;
C.次氯酸具有强的氧化性能够氧化亚硫酸氢根离子生成硫酸根离子;
D.二者的物质的量比为2:5,反应生成氢氧化铝和氯化铝.
解答 解:A.用碳酸钠溶液吸收少量二氧化硫,离子方程式:2 CO32-+SO2+H2O=2 HCO3-+SO32-,故A正确;
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀,离子方程式为:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓,故B正确;
C.0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合,由题目可知次氯酸钠过量,反应生成SO42-、Cl-和HClO,反应的离子方程式为:HSO3-+2ClO-=SO42-+Cl-+HClO,故C错误;
D.偏铝酸钠与盐酸按照物质的量之比2:3反应生成氢氧化铝和氯化铝,离子方程式:6 AlO2-+9H++6H2O=5Al(OH)3↓+Al3+,故D正确.
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质和离子方程式书写方法是解题关键,注意反应物用量对反应的影响,选项D为易错选项.

练习册系列答案
相关题目
10.气体摩尔体积在同温、同压下相等的本质原因是在同温、同压下( )
| A. | 气体体积的大小只随分子数变化 | |
| B. | 不同气体分子的大小几乎相等 | |
| C. | 不同气体分子间的平均距离几乎相等 | |
| D. | 气体分子的平均距离与分子本身大小成正比 |
11.能鉴别CO2和SO2的试剂是( )
| A. | 品红溶液 | B. | 澄清石灰水 | ||
| C. | 紫色石蕊试液 | D. | 氯化钡溶液和氯水 |
8.在标准状况下,H2和Cl2各nL,经混合光照反应后,所得气体恰好使bmolNaOH完全转化为盐,n与b的关系可能是( )
| A. | b=$\frac{n}{22.4}$ | B. | b=$\frac{22.4}{n}$ | C. | b=$\frac{n}{11.2}$ | D. | b=11.2n |
15.向质量分数为2a%,体积为10mL物质的量浓度为c1 mol•L-1的稀H2SO4中加入V mL的水,使之质量分数变为a%,此时物质的量浓度为c2 mol•L-1,则下列关系正确的是( )
| A. | V>10 2c2=c1 | B. | V<10 2c2>c1 | C. | V>10 2c2<c1 | D. | V>10 2c2>c1 |
5.某恒温密闭容器中,可逆反应A(s)?B+C(g)-Q达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )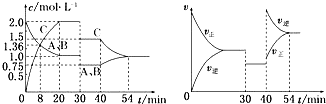

| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗:n(C)消耗=1:1 | |
| C. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 | |
| D. | 若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q |
9.碳化硅(SiC)是一种晶体,具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的,在下列三种晶体中:①金刚石,②晶体硅,③碳化硅,它们的熔点由高到低的是( )
| A. | ①③② | B. | ③②① | C. | ②③① | D. | ②①③ |
10.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:铝>氧化铝 |
| B | 某酸雨试样中加入Ba(OH)2溶液 | 产生白色沉淀 | 酸雨试样中只含SO42- |
| C | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸变黑 | 浓硫酸具有脱水性 |
| D | 食用加碘盐加入食醋和KI溶液,再加入CCl4振荡,静置 | 下层呈紫红色 | 该食用加碘盐含有KIO3 |
| A. | A | B. | B | C. | C | D. | D |