题目内容
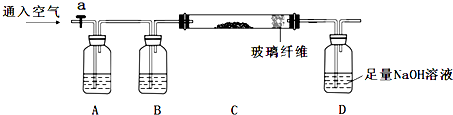
3.下列实验步骤是兴趣小组对某混合样品含量的测定,样品成分为FeO、FeS2、SiO2、及其它杂质,杂质不与酸碱反应,受热稳定.(步骤中所加试剂均为足量)①称量m g样品灼烧.装置如下:
②D瓶溶液$\stackrel{H_{2}O_{2}溶液}{→}$$\stackrel{BaCl_{2}溶液}{→}$$\stackrel{连续操作1}{→}$固体(ag)
③
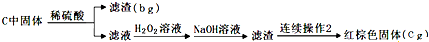
请回答下列问题:
(1)连接好仪器后,如何检查整套装置的气密性向D中加水浸没导管,夹紧止水夹a,微热C,导管口有气泡,停止微热后,若D导管中形成一段稳定的水柱,则气密性良好.
(2)A瓶内所盛试剂是氢氧化钠溶液.灼烧完成后熄灭酒精灯,若立即停止通空气,可能对实验的影响是(写两点)D中溶液倒吸、SO2不能全部排出或测得硫元素的含量偏低.
(3)步骤②中加入双氧水的离子方程式为SO32-+H2O2=SO42-+H2O.若此步骤不加入双氧水对测定硫元素含量的影响是偏高(填“偏高”、“偏低”或“无影响”).
(4)连续操作1为过滤、洗涤、干燥、称量;连续操作2为洗涤、灼烧、称量.
(5)从步骤③的bg滤渣入手,可测定SiO2的含量,下面各组试剂中不适合测定的是BC.
A.NaOH溶液、稀硫酸
B.Ba(OH)2溶液、盐酸
C.氨水、稀硫酸
D.NaOH溶液、盐酸
(6)求样品中FeO的质量分数(列出算式即可)$\frac{(\frac{c}{160}×2-\frac{a}{233}×\frac{1}{2})×72}{m}×100%$.
分析 样品成分为FeO、FeS2、SiO2、及其它杂质,杂质不与酸碱反应,受热稳定,mg样品灼烧FeS2燃烧生成Fe2O3和SO2
①A瓶是氢氧化钠溶液吸收空气中的二氧化碳等酸性气体,B装置是浓硫酸干燥气体,C装置是样品灼烧得到氧化铁固体和二氧化硅,装置D是吸收生成的二氧化硫气体生成亚硫酸钠;
②D瓶中加入过氧化氢氧化亚硫酸钠为硫酸钠,加入氯化钡溶液形成硫酸钡沉淀,过滤、洗涤、干燥得到固体为BaSO4ag;
③C中固体为FeO、Fe2O3和SiO2和其他杂质,加入稀硫酸溶解生成硫酸亚铁、硫酸铁溶液,过滤得到滤渣为SiO2和其他杂质bg,滤液中加入过氧化氢氧化亚铁离子为铁离子,加入氢氧化钾溶液沉淀铁离子为Fe(OH)3,过滤得到滤渣洗涤干燥后灼烧得到红褐色固体Fe2O3质量为cg;
(1)连接好仪器后,关闭紧止水夹a,微热C检查整套装置的气密性,依据导气管气泡冒出,停止加热导气管中有水柱上升证明气密性完好;
(2)上述分析可知A为氢氧化钠溶液用来吸收空气中二氧化碳避免影响后续实验测定,灼烧完成后熄灭酒精灯,若立即停止通空气,可能会引起倒吸,生成的二氧化硫不能全部进入装置D中吸收;
(3)过氧化氢是氧化亚硫酸根离子为硫酸根离子全部沉淀,如不加入过氧化氢氧化,生成的沉淀含有BaSO3,称量过程中易被空气中氧气氧化,计算得到硫元素质量偏高;
(4)依据上述分析的连续操作1是过滤、洗涤、干燥、称量;连续操作2是洗涤、干燥、灼烧、称量;
(5)C中固体为FeO、Fe2O3和SiO2和其他杂质,加入稀硫酸溶解生成硫酸亚铁、硫酸铁溶液,过滤得到滤渣为SiO2和其他杂质bg,杂质不与酸碱反应,受热稳定,分离后测定SiO2的含量的方法是:溶解二氧化硅后过滤,得到不溶杂质固体,滤液中加入酸生成硅酸沉淀,元素守恒计算得到二氧化硅的质量,据此计算二氧化硅含量;
(6)样品成分为FeO、FeS2、SiO2、及其它杂质,依据铁元素守恒分析计算,实验③中得到的固体是氧化铁质量为cg,实验②是FeS2中硫元素最后生成硫酸钡沉淀为ag,据此可以依据硫元素守恒计算原样品中FeS2的物质的量,原样品中FeO物质的量应是铁元素总物质的量减去FeS2中铁元素物质的量,得到氧化亚铁的质量分数.
解答 解:样品成分为FeO、FeS2、SiO2、及其它杂质,杂质不与酸碱反应,受热稳定,mg样品灼烧FeS2燃烧生成Fe2O3和SO2
①A瓶是氢氧化钠溶液吸收空气中的二氧化碳等酸性气体,B装置是浓硫酸干燥气体,C装置是样品灼烧得到氧化铁固体和二氧化硅,装置D是吸收生成的二氧化硫气体生成亚硫酸钠;
②D瓶中加入过氧化氢氧化亚硫酸钠为硫酸钠,加入氯化钡溶液形成硫酸钡沉淀,过滤、洗涤、干燥得到固体为BaSO4ag;
③C中固体为FeO、Fe2O3和SiO2和其他杂质,加入稀硫酸溶解生成硫酸亚铁、硫酸铁溶液,过滤得到滤渣为SiO2和其他杂质bg,滤液中加入过氧化氢氧化亚铁离子为铁离子,加入氢氧化钾溶液沉淀铁离子为Fe(OH)3,过滤得到滤渣洗涤干燥后灼烧得到红褐色固体Fe2O3质量为cg;
(1)检查整套装置的气密性,先连接好仪器后,关闭紧止水夹a,微热C,依据导气管气泡冒出,停止加热导气管中有水柱上升证明气密性完好,具体步骤为:向D中加水浸没导管,夹紧止水夹a,微热C,导管口有气泡,停止微热后,若D导管中形成一段稳定的水柱,则气密性良好;
故答案为:向D中加水浸没导管,夹紧止水夹a,微热C,导管口有气泡,停止微热后,若D导管中形成一段稳定的水柱,则气密性良好;
(2)上述分析可知A中是氢氧化钠溶液,用来吸收通入空气中二氧化碳,避免影响后续实验测定,灼烧完成后熄灭酒精灯,若立即停止通空气,可能会引起倒吸,生成的二氧化硫不能全部进入装置D中吸收等;
故答案为:氢氧化钠,D中溶液倒吸、SO2不能全部排出或测得硫元素的含量偏低;
(3)过氧化氢是氧化亚硫酸根离子为硫酸根离子全部沉淀,步骤②中加入双氧水的离子方程式为:SO32-+H2O2=SO42-+H2O,如不加入过氧化氢氧化,生成的沉淀含有BaSO3,称量过程中易被空气中氧气氧化,计算得到硫元素质量偏高;
故答案为:SO32-+H2O2=SO42-+H2O,偏高;
(4)依据上述分析可知,实验过程中连续操作1是过滤、洗涤、干燥、称量;连续操作2是洗涤、干燥、灼烧、称量;
故答案为:过滤,干燥,灼烧;
(5)③C中固体为FeO、Fe2O3和SiO2和其他杂质,加入稀硫酸溶解生成硫酸亚铁、硫酸铁溶液,过滤得到滤渣为SiO2和其他杂质bg,杂质不与酸碱反应,受热稳定,从步骤③的bg滤渣入手,可测定SiO2的含量是利用加入的试剂溶解二氧化硅后过滤得到不溶性杂质,滤液中加入酸沉淀硅酸根离子形成硅酸沉淀,洗涤干燥称量,元素守恒计算得到二氧化硅质量,得到二氧化硅的含量;
A.NaOH溶液、以溶解二氧化硅,稀硫酸和硅酸钠反应生成硅酸沉淀,可以测定二氧化硅含量,故A符合;
B.Ba(OH)2溶液和二氧化硅反应生成硅酸钡是沉淀,不能和杂质分离、不能用来测定含量,故B不符合;
C.氨水不能溶解二氧化硅,不能分离不溶性杂质,故C不符合;
D.NaOH溶液、以溶解二氧化硅,稀盐酸和硅酸钠反应生成硅酸沉淀,可以测定二氧化硅含量,故D符合;
故答案为:BC;
(6)依据铁元素守恒分析计算,实验③中得到的固体是氧化铁质量为cg,实验②是FeS2中硫元素最后生成硫酸钡沉淀为ag,据此可以依据硫元素守恒计算原样品中FeS2的物质的量,原样品中FeO物质的量应是铁元素总物质的量减去FeS2中铁元素物质的量,氧化铁物质的量=$\frac{cg}{160g/mol}$=$\frac{c}{160}$mol,含有铁元素物质的量=$\frac{c}{160}$mol×2,依据硫元素守恒,Fe~FeS2~2H2SO4~2BaSO4,则FeS2中铁元素物质的量=$\frac{a}{233}$×$\frac{1}{2}$mol
氧化亚铁FeO中铁元素物质的量=$\frac{c}{160}$mol×2-$\frac{a}{233}$×$\frac{1}{2}$mol
得到氧化亚铁的质量分数为:$\frac{(\frac{c}{160}×2-\frac{a}{233}×\frac{1}{2})×72}{m}×100%$;
故答案为:$\frac{(\frac{c}{160}×2-\frac{a}{233}×\frac{1}{2})×72}{m}×100%$;
点评 本题考查了物质组成的实验探究方法和实验过程分析判断,元素守恒的计算应用,物质性质和实验基本操作是解题关键,题目难度较大.

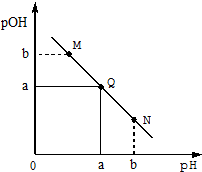 某温度下,向一定体积0.1mol/LHCl溶液中逐滴加入等浓度的氨水溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如右图所示,则下列
某温度下,向一定体积0.1mol/LHCl溶液中逐滴加入等浓度的氨水溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如右图所示,则下列说法错误的是( )
| A. | Q点消耗氨水溶液的体积等于HCl溶液的体积 | |
| B. | M点所示溶液导电能力弱于Q点 | |
| C. | M点和N点所示溶液中水的电离程度相同 | |
| D. | N点所示溶液中c(NH4+)>c(OH-) |
| A. | 0.1 mol•L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1 mol•L-1NaHCO3溶液与0.1 mol•L-1NaOH溶液等体积混合:c(Na+)=2c(CO32-)+c(HCO3-)+2c(H2CO3) | |
| C. | 0.1 mol•L-1NaHCO3溶液与0.2 mol•L-1NaOH溶液等体积混合:c(Na+)>c(OH-)>0.05 mol•L-1>c(CO32-)>c(HCO3-) | |
| D. | 0.2 mol•L-1NaHCO3溶液与0.1 mol•L-1NaOH溶液等体积混合:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
| A. | 重金属离子Ag+、Cu2+、K+均可导致蛋白质变性 | |
| B. | S02和NxOy都属于非金属氧化物,也都是酸性氧化物 | |
| C. | 部分颗粒分散在空气中可能会形成丁达尔现象 | |
| D. | 苯和苯的衍生物都是芳香烃 |
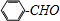 ;
; ;②
;②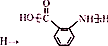 :
: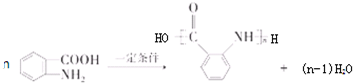 ;
;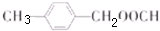 ;
;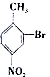 合成
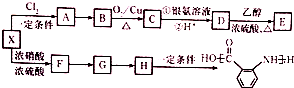
合成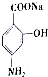 的转化流程图(写出反应物和反应条件).
的转化流程图(写出反应物和反应条件).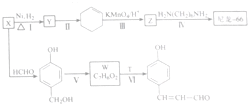

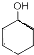 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O,反应类型为消去反应
+H2O,反应类型为消去反应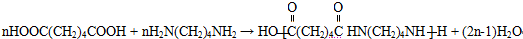 ,反应类型为缩聚反应
,反应类型为缩聚反应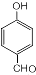 ,T的分子式为C2H4O
,T的分子式为C2H4O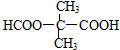 .
. 实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定氢氧化钠的质量分数约为82%,为了验证其纯度,用浓度为0.2mol•L-1的盐酸进行滴定,完成下列问题:
实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定氢氧化钠的质量分数约为82%,为了验证其纯度,用浓度为0.2mol•L-1的盐酸进行滴定,完成下列问题: