题目内容
在一定温度下,反应:2A(s)+2B(g)  C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是
| A.单位时间内生成2a mol B,同时生成a molD |
| B.C的质量不再改变 |
| C.容器内的压强不随时间而变化 |
| D.混合气体的密度不再随时间而变化 |
C
解析试题分析:对于一个可逆反应,达到化学平衡,说明正反应速率与逆反应速率相等。且各物质的浓度保持不变,A选项如果从速率来判断一个反应是否达到平衡,需要有正的反应方向和逆的反应方向,且生产和消耗的反应速率要等于化学计量数。单位时间内生成2a mol B,反应方向为逆反应方向,,生成a molD,反应方向为正反应方向,且比例关系是按化学计量数进行的,因此A选项是能说明该反应已达到化学平衡状态的。B选项C的质量不再改变,说明其他物质的质量也是不变的,因此B选项也是正确的。C选项。左边反应物的气体量为2,右边生成物的气体量也为2.说明在任何的情况下,容器内的压强都是不会发生变化的,所以C选项是错误的。D选项,密度等于质量处于体积,据质量守恒定律可知,反应前后物质的总质量不变,而反应物中,有固体物质,因为如果反应向正反应方向进行的时候,气体的质量增大,反应向逆反应方向进行的时候,气体的质量减小,而反应前后气体的体积不变,气体质量的改变必定会造成气体密度的改变,因为如果混合气体的密度不再随时间而变化说明个物质的浓度保持不变,所以D选项是正确的。
考点:考查化学平衡的相关知识点

 考前必练系列答案
考前必练系列答案氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO +3HSO
+3HSO ===3SO
===3SO +Cl-+3H+,已知该反应的速率随溶液酸性的增强而加快。下图为用ClO
+Cl-+3H+,已知该反应的速率随溶液酸性的增强而加快。下图为用ClO 在单位时间内的物质的量浓度的变化来表示该反应的速率一时间图象。下列说法不正确的是( )
在单位时间内的物质的量浓度的变化来表示该反应的速率一时间图象。下列说法不正确的是( )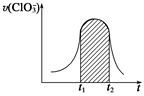
| A.反应开始时速率增大可能是c(H+)增大引起的 |
| B.纵坐标为v(H+)的速率—时间曲线与图中曲线能完全重合 |
| C.后期反应速率下降的主要原因是反应物的浓度减小 |
D.图中的阴影部分“面积”为t1~t2时间内ClO 的物质的量浓度的减小值 的物质的量浓度的减小值 |
关于化学平衡常数、电离平衡常数、水的离子积常数和溶解平衡常数,下列说法正确的是
| A.四种平衡常数都是一个比值,没有单位 |
| B.四种平衡常数都是温度的函数,温度升高其值都增大 |
| C.一个化学反应的平衡常数与物质的计量数无关 |
| D.对于同类型反应,化学平衡常数K的大小反映了化学反应可能进行的程度 |
在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:
A(s)+2B(g) C(g)+D(g) 已达平衡的是
C(g)+D(g) 已达平衡的是
| A.混合气体的压强 | B.混合气体的密度 |
| C.生成l mol C的同时生成l mol D | D.气体的总物质的量 |
可逆反应A(g)+ 4B(g) C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
| A.vA==0.15mol/(L·min) | B.vB="=0.6" mol/(L·min) |
| C.vC="=0.4" mol/(L·min) | D.vD="=0.01" mol/(L·s) |
 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是 3C+5D反应中,表示该反应速率最快的是
3C+5D反应中,表示该反应速率最快的是