题目内容
4.新闻:美国《科学》杂志12月17日评选出2004十大科学突破中,有多项与水有关,其中之一是关于对水的研究有新进展,一些科学家对于水分子如何聚合以及电子及质子如何在水中溶解等问题上,都有了新发现.另据 2004年4月14日中科院网报道,中科院物理所王恩哥小组他们首次证明存在一种稳定的二维冰相.它是由四角形和八角形的氢键网格交替组成的,研究人员把这种新的冰结构命名为镶嵌冰.有趣的是,这种镶嵌冰可以在室温下稳定存在.有关这种镶嵌冰的推测肯定不正确的( )| A. | 镶嵌冰密度不可能比4℃水大 | |
| B. | 镶嵌冰中四角形环比八角形环中水分间的氢键键能强 | |
| C. | 每个水分子形成两个氢键 | |
| D. | 镶嵌冰属于分子晶体 |
分析 A.镶嵌冰中的氢键比液态水中的强,使得水分子排列得很规则,造成体积膨胀,密度变小;
B.四角形环比八角形环中水分子间的氢键键能强;
C.每个水分子含有两个O-H键,故每个水分子可形成4个氢键;
D.镶嵌冰是由水分子构成的,属于分子晶体.
解答 解:A.镶嵌冰中的氢键比液态水中的强,使得水分子排列得很规则,造成体积膨胀,密度变小,故镶嵌冰密度不可能比4℃水大,故A正确;
B.四角形环比八角形环中水分子间的氢键键能强,故B正确;
C.每个水分子含有两个O-H键,故每个水分子可形成4个氢键,故C错误;
D.镶嵌冰是由水分子构成的,属于分子晶体,故D正确;
故选C.
点评 本题考查氢键的相关知识,难度较大.要注意在冰中,每个水分子周围紧邻4个水分子.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.最近,意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子O4,并用质谱仪探测到了它存在的证据.下列说法正确的是( )
| A. | 18O是氧元素的一种核素,它的中子数是8 | |
| B. | O4和O2是互为同位素 | |
| C. | 同温同压下,等体积的O4气体和O2含有相同的分子数 | |
| D. | O4转化O2为物理性质 |
12.下列各组数据中比值不为1:1的是( )
| A. | 100℃时,pH=6的纯水中,c(OH-)与c(H+)之比 | |
| B. | 常温下,pH=1的HF溶液与0.1mol•L-1的盐酸中c(H+)之比 | |
| C. | 常温下,pH=7的CH3COOH与CH3COONa的混合溶液中,c(CH3COO-)与c(Na+)之比 | |
| D. | 常温下,pH=12的Ba(OH)2溶液与pH=12的KOH溶液中溶质的物质的量浓度之比 |
19.室温下,将1molNa2CO3•10H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1molNa2CO3(s)溶于水会使溶液温度升高,热效应为△H2;Na2CO3•10H2O受热分解的化学方程为:Na2CO3•10H2O(s)$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3(s)+10H2O(l),热效应为△H3,则下列判断正确的是( )
| A. | △H2<△H3 | B. | △H1>△H3 | C. | △H1+△H3=△H2 | D. | △H1+△H2>△H3 |
9.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 标准状况下,11.2L乙醇完全燃烧所生成的气态产物的分子数为NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5摩尔硅中含有的化学键数目为NA | |
| D. | 1 mo CH3+所含的电子总数为8NA |
16.下列关于化学键的叙述,正确的一项是( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均存在化学键 | |
| C. | 含有非极性共价键的分子一定是单质分子 | |
| D. | 含有共价键的化合物一定是共价化合物 |
13.下列各组比较不正确的是( )
| A. | 锂与水反应不如钠与水反应剧烈 | |
| B. | 还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠 | |
| C. | 熔沸点:Li>Na>K | |
| D. | 原子半径:Li<Na<K |
5.下列表示物质或微粒的化学用语或模型正确的是( )
| A. | 氮分子的结构式:N-N | B. | Mg2+的结构示意图: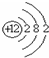 | ||
| C. | 二氧化碳电子式 | D. | 钙离子的电子式:Ca2+ |