题目内容
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量)。
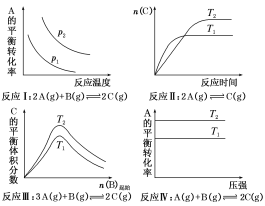
根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:ΔH>0,p2>p1B.反应Ⅱ:ΔH<0,T1<T2
C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1D.反应Ⅳ:ΔH<0,T2>T1
【答案】C
【解析】
A. 反应Ⅰ中,由图分析,升温,A的平衡转化率降低,平衡逆移,而升温,平衡向吸热方向移动,所以反应是放热反应ΔH<0。因为反应I是体积减小的可逆反应,即压强越大,反应物的转化率越高,P2>P1, A错误;
B. 反应Ⅱ中,根据先拐先平衡,数值大,故T1>T2,B错误;
C. 反应Ⅲ中,如ΔH>0,T2>T1,则升高温度平衡向正反应方向移动,C的体积分数增大,如ΔH<0,T2<T1,则升高温度,平衡向逆反应方向移动,C的体积分数减小,与图象吻合,C正确;
D. 反应Ⅳ中如ΔH<0,则升高温度平衡向逆反应方向移动,A的转化率减小,则T2<T1,D错误。
答案选C。

【题目】研究电解质在水溶液中的平衡能了解它的存在形式。
(1)已知部分弱酸的电离常数如下表:
化学式 | HF | H2CO3 | H2S |
电离平衡常数K(25℃) |
|
|
|
①写出H2S的Ka1的表达式:________________。
②常温下,pH相同的三种溶液NaF、Na2CO3、Na2S,物质的量浓度最小的是_______。
③将过量H2S通入Na2CO3溶液,反应的离子方程式是_______________。
(2)室温下,用0.100 mol·L-1 盐酸溶液滴定20.00 mL 0.100 mol·L-1 的氨水溶液,滴定曲线如图所示。(忽略溶液体积的变化,①②填“>”“<”或“=”)
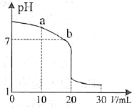
①a点所示的溶液中c(NH3·H2O)___________c(Cl-)。
②b点所示的溶液中c(Cl-)___________c(NH4+)。
③室温下pH=11的氨水与pH=5的NH4Cl溶液中,由水电离出的c(H+)之比为__________。
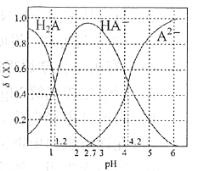
(3)二元弱酸H2A溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示。则H2A第二级电离平衡常数Ka2=___________。