题目内容
【题目】丹参醇是一种中药成分,结构简式如图所示。下列关于丹参醇的描述正确的是

A.能与浓硫酸共热后发生消去反应
B.能与NaHCO3溶液反应放出气体
C.分子中含有2个手性碳原子
D.1 mol丹参醇最多能与5 mol H2发生加成反应
【答案】AC
【解析】
观察丹参醇的分子式可知,该分子含羟基、羰基、醚键和碳碳双键;连有4个不同基团的碳原子是手性碳原子。可在此基础上对各选项作出判断。
A. 丹参醇的分子含羟基,且羟基连的碳相邻的碳上有H,所以,能与浓硫酸共热后发生消去反应,A选项正确;
B. 丹参醇的分子中官能团为醇羟基、羰基、醚键,碳碳双键,均不能与NaHCO3溶液反应,B选项错误;
C. 如图“*”所示: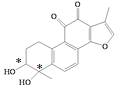 ,丹参醇的分子中含有2个手性碳原子, C选项正确;
,丹参醇的分子中含有2个手性碳原子, C选项正确;
D. 该分子含1个苯环、2个羰基、和2个碳碳双键,可与7分子H2加成,所以1 mol丹参醇最多能与7 mol H2发生加成反应,D选项错误;
答案选AC。

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
【题目】一定条件下,两体积均为1 L的容器中发生反应:CO(g)+2H2(g) ![]() CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
CH3OH(g) ΔH。容器中起始各物质的物质的量如下表所示,两容器中c(H2)随时间t的变化如下图所示。
容器 | 温度 | CO | H2 | CH3OH |
Ⅰ | T1℃ | a mol | 2 mol | 0 mol |
Ⅱ | T1℃ | 0.5 mol | 1 mol | 0 mol |

下列说法正确的是
A.0~5 min时,容器Ⅰ中v(CO)=0.1 mol·L-1·min-1
B.a>1
C.若容器Ⅱ温度改变为T2(T2>T1)时,平衡常数K=1,则ΔH<0
D.T1℃时,若向容器Ⅰ中充入CO、H2、CH3OH各1 mol,反应将向逆反应方向进行