题目内容
【题目】某高铬型钒渣含Fe2O3、Fe3O4、SiO2、Al2O3、V2O5、Cr2O3等物质,从中分离提取钒和铬的工艺流程如图所示:
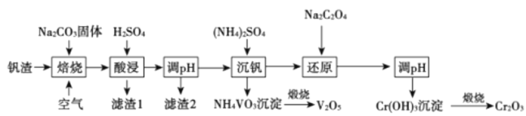
回答下列问题:
(1)“焙烧”时V2O5、Cr2O3转化为NaVO3和Na2CrO4,SiO2、Al2O3转化为________和_______。
(2)滤渣1中主要含______。 滤渣2的主要成分是Fe(OH)3和Al(OH)3,对应调pH应不低于______。(常温下,当溶液中离子浓度小于1×10-5mol/L时认为沉淀完全, Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=1.0×10-33)。
(3)“沉钒”时的离子方程式是_______,NH4VO3煅烧过程中的化学方程式是______。
(4)“还原”时溶液的pH在2.5左右,反应的离子方程式是________。
(5)已知:25 °C时,H2C2O4的电离常数Ka1=5.9×10-2,Ka2=6. 4×10-5,则25° C时,0.1 mol·L-1NaHC2O4溶液中各离子浓度由大到小的顺序为_____,向0.1 mol· L-1H2C2O4溶液中加入一定的NaOH固体,当溶液的pH= 2.5时,溶液中c(C2O42-) :c(H2C2O4)=_______(保留两位有效数字)。
【答案】Na2SiO3 NaAlO2 H2SiO3 4.7 NH4++VO3-=NH4VO3↓ 2NH4VO3![]() V2O5+2NH3↑+H2O↑ 3C2O42-+2CrO42-+16H+= 2Cr3++6CO2↑+8H2O c(Na+)>c(HC2O4-)>c(H+)>C2O42->c(OH-) 0.38
V2O5+2NH3↑+H2O↑ 3C2O42-+2CrO42-+16H+= 2Cr3++6CO2↑+8H2O c(Na+)>c(HC2O4-)>c(H+)>C2O42->c(OH-) 0.38
【解析】
“焙烧”时,Fe2O3、Fe3O4不和Na2CO3、O2反应,V2O5、Cr2O3和Na2CO3、O2反应转化为NaVO3、Na2CrO4,SiO2、Al2O3和Na2CO3反应转化成Na2SiO3、NaAlO2;
“酸浸”时,Na2SiO3和硫酸反应生成H2SiO3沉淀,滤渣1主要成分是硅酸,同时AlO2-转化成Al3+,铁的两种氧化物溶于酸得到Fe2+和Fe3+;
“调pH”时,将铝元素、铁元素转化为Al(OH)3和Fe(OH)3沉淀,滤渣2主要成分为Al(OH)3和Fe(OH)3;
“沉钒”时,NH4+和VO3-形成NH4VO3沉淀,NH4VO3沉淀煅烧得V2O5;
“还原”时,用Na2C2O4将CrO42-还原成Cr3+,调合适的pH将Cr3+转化为Cr(OH)3沉淀,Cr(OH)3沉淀煅烧得到Cr2O3,据以上分析解答。
(1) 高温时,氧化铝和碳酸钠反应生成偏铝酸钠和二氧化碳,二氧化硅和碳酸钠反应生成硅酸钠和二氧化碳,即SiO2、Al2O3转化为Na2SiO3和NaAlO2,故答案为:Na2SiO3;NaAlO2;
(2)由分析可知,滤渣1主要为H2SiO3,Ksp[Fe(OH)3]=4.0×10-38,Fe3+浓度小于1×10-5mol/L时认为沉淀完全,Fe3+浓度为1×10-5mol/L时,c3(OH-)×1×10-5mol/L=4.0×10-38,c3(OH-)=4.0×10-33,c3(H+)=![]() ,c(H+)=
,c(H+)=![]() ×10-4≈6×10-4,pH≈4-lg6<4。Al3+浓度为1×10-5mol/L时,c3(OH-)×1×10-5mol/L=1.0×10-33,c3(OH-)=1.0×10-28,c3(H+)=
×10-4≈6×10-4,pH≈4-lg6<4。Al3+浓度为1×10-5mol/L时,c3(OH-)×1×10-5mol/L=1.0×10-33,c3(OH-)=1.0×10-28,c3(H+)=![]() ,c(H+)=
,c(H+)=![]() ,pH=-lg(
,pH=-lg(![]() )=5- lg(
)=5- lg(![]() )≈4.7>4,综上所述,要使A3+和Fe3+完全沉淀,p不低于4.7,故答案为:H2SiO3;4.7;
)≈4.7>4,综上所述,要使A3+和Fe3+完全沉淀,p不低于4.7,故答案为:H2SiO3;4.7;
(3)“沉钒”时,NH4+和VO3-形成NH4VO3沉淀,离子方程式为:NH4++VO3-=NH4VO3↓,NH4VO3沉淀煅烧得到V2O5,元素化合价没变化,根据原子守恒可知,产物含有H2O和NH3,方程式为:2NH4VO3![]() V2O5+2NH3↑+H2O↑,故答案为:NH4++VO3-=NH4VO3↓;2NH4VO3
V2O5+2NH3↑+H2O↑,故答案为:NH4++VO3-=NH4VO3↓;2NH4VO3![]() V2O5+2NH3↑+H2O↑;
V2O5+2NH3↑+H2O↑;
(4) “还原”时,C2O42-将CrO42-还原成Cr3+,pH在2.5左右,溶液为酸性,C2O42-被氧化为CO2,结合电子得失守恒、原子守恒可得离子方程式为:3C2O42-+2CrO42-+16H+= 2Cr3++6CO2↑+8H2O,故答案为:3C2O42-+2CrO42-+16H+= 2Cr3++6CO2↑+8H2O;
(5) HC2O4-会水解、电离,所以,c(Na+)>c(HC2O4-),HC2O4-的电离常数= Ka2=6. 4×10-5,HC2O4-的水解常数Kh=![]() =
=![]() ≈1.7×10-13,电离常数>>水解常数,加之水电离也能产生一定的H+,所以c(H+)>C2O42->c(OH-)。水解和电离都是微弱的,所以,c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-),综上所述:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)。H2C2O4
≈1.7×10-13,电离常数>>水解常数,加之水电离也能产生一定的H+,所以c(H+)>C2O42->c(OH-)。水解和电离都是微弱的,所以,c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-),综上所述:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)。H2C2O4![]() H++HC2O4-,Ka1=
H++HC2O4-,Ka1=![]() ,HC2O4-
,HC2O4-![]() H++C2O42-,Ka2=
H++C2O42-,Ka2=![]() ,Ka1×Ka2=
,Ka1×Ka2=![]() ×
×![]() =
=![]() 。pH= 2.5,则c(H+)=10-2.5,所以,
。pH= 2.5,则c(H+)=10-2.5,所以,![]() =
=![]() =0.38(保留两位有效数字),即c(C2O42- ):c(H2C2O4)=0.38,故答案为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);0.38;
=0.38(保留两位有效数字),即c(C2O42- ):c(H2C2O4)=0.38,故答案为:c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);0.38;

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中非金属元素原子的电负性大小顺序是__。基态K+的电子排布式为__。
(2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是__,中心原子的杂化方式为__。NaBH4中存在__(填标号)。
a.离子键 b.氢键 c.σ键 d.π键
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为__,其中Be的配位数为__。
(4)第三周期元素氟化物的熔点如下表:
化合物 | NaF | MgF2 | AlF3 | SiF4 | PF5 | SF6 |
熔点/℃ | 993 | 1261 | 1291 | -90 | -83 | -50.5 |
解释表中氟化物熔点变化的原因:___。
(5)CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,若r(F-)=xpm,r(Ca2+)=ypm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=__g·cm-3(列出计算表达式)。