题目内容
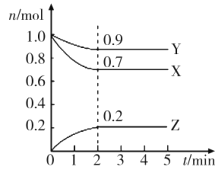
【题目】两气体A、B分别为0.6mo1与0.5mo1,在0.4L密闭容器中发生反应:3A+BmC+2D(C、D均为气态物质),经5min后达到平衡,此时C为0.2mo1,在此时间内D的平均反应速率为0.1mo1L-1min-1,下列结论错误的是( )
A.平衡时反应混合物总物质的量为1mo1
B.B的转化率为20%
C.A的平均反应速率为0.15mo1L-1min-1
D.m值为2
【答案】A
【解析】
经5min后达到平衡,此时C为0.2mol,v(C)= =0.1mol·L-1·min-1,又知在此反应时间D的平均反应速率为0.1mol·L-1·min-1,由反应速率之比等于化学计量数之比可知m=2,则
=0.1mol·L-1·min-1,又知在此反应时间D的平均反应速率为0.1mol·L-1·min-1,由反应速率之比等于化学计量数之比可知m=2,则

据此分析。
A.平衡时混合物总物质的量为:0.3mol+0.4mol+0.2mol+0.2mol=1.1mol,故A错误;
B.平衡时B的转化率为:![]() ×100%=20%,故B正确;
×100%=20%,故B正确;
C.A的平均反应速率为 =0.15 molL﹣1min﹣1,故C正确;
=0.15 molL﹣1min﹣1,故C正确;
D.根据分析可知,m=2,故D正确;
答案选A。

练习册系列答案
相关题目