جâؤ؟ؤعبف
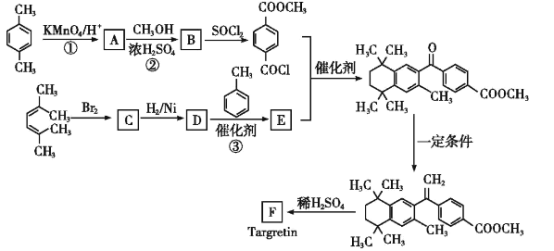
،¾جâؤ؟،؟ز©خïTargretin£¨F£©ؤـضخءئحç¹جذشئ¤·ôTد¸°ûءـ°حءِ£¬ئن؛د³ةآ·دكبçح¼ثùت¾£؛
زرضھ£؛
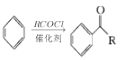
¢،.
¢¢.![]()
¢£.RCOOH![]() RCOCl£¨R±يت¾ج»ù£©
RCOCl£¨R±يت¾ج»ù£©
£¨1£©·´س¦¢ظµؤ·´س¦ہàذحتا__،£
£¨2£©·´س¦¢عµؤ»¯ر§·½³جت½£؛__،£
£¨3£©Cµؤ؛ث´إ¹²صٌاâئ×ح¼ضذسذ__¸ِ·ه،£
£¨4£©·´س¦¢غµؤ»¯ر§·½³جت½£؛__،£
£¨5£©Fµؤ·ض×ست½تاC24H28O2،£Fضذ؛¬سذµؤ¹ظؤـحإ£؛__،£
£¨6£©ذ´³ِآْ×مدآءذجُ¼Aµؤء½ضضح¬·ضزى¹¹جهµؤ½ل¹¹¼ٍت½£¨²»؟¼آا-O-O-»ٍ![]() ½ل¹¹£©£؛__،£
½ل¹¹£©£؛__،£
a.±½»·ةدµؤز»آب´ْخïسذء½ضض
b.¼بؤـ·¢ةْزّ¾µ·´س¦سضؤـ·¢ةْث®½â·´س¦
£¨7£©زرضھ£؛![]() £¨R،¢R،نخھج»ù£©،£زش2-نه±ûحé؛حززد©خھشءد£¬ر،سأ±طزھµؤخق»ْتش¼ء؛د³ة
£¨R،¢R،نخھج»ù£©،£زش2-نه±ûحé؛حززد©خھشءد£¬ر،سأ±طزھµؤخق»ْتش¼ء؛د³ة![]() £¬ذ´³ِ؛د³ةآ·دك__£¨سأ½ل¹¹¼ٍت½±يت¾سذ»ْخسأ¼ح·±يت¾×ھ»¯¹طدµ£¬¼ح·ةد×¢أ÷تش¼ء؛ح·´س¦جُ¼،£
£¬ذ´³ِ؛د³ةآ·دك__£¨سأ½ل¹¹¼ٍت½±يت¾سذ»ْخسأ¼ح·±يت¾×ھ»¯¹طدµ£¬¼ح·ةد×¢أ÷تش¼ء؛ح·´س¦جُ¼،£
،¾´ً°¸،؟رُ»¯·´س¦ ![]() +CH3OH
+CH3OH![]()
![]() +H2O 2 (CH3)2CBr-CH2CH2-BrC(CH3)2+
+H2O 2 (CH3)2CBr-CH2CH2-BrC(CH3)2+![]()
![]()
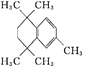 +2HBr ج¼ج¼ث«¼ü،¢ôب»ù
+2HBr ج¼ج¼ث«¼ü،¢ôب»ù ![]() ،¢
،¢![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br
BrCH2CH2Br![]() HOCH2CH2OH
HOCH2CH2OH![]() OHC-CHO
OHC-CHO![]()

![]()
![]()
،¾½âخِ،؟
¶ش¶¼×±½±»ثلذش¸كأجثل¼طرُ»¯خھAتا¶ش±½¶¼×ثل£¬¶ش±½¶¼×ثلسë¼×´¼·¢ةُْ¥»¯·´س¦ةْ³ةBتا £¬¸ù¾فزرضھ¢£؟ةضھ£¬BسëSOCl2·´س¦ةْ³ة
£¬¸ù¾فزرضھ¢£؟ةضھ£¬BسëSOCl2·´س¦ةْ³ة £»
£»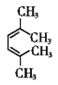 سëنه·¢ةْ1£¬4-¼س³ة·´س¦ةْ³ةCخھ(CH3)2CBr-CH=CH-BrC(CH3)2£¬¸أسذ»ْخïسëاâئّ·¢ةْ¼س³ة·´س¦ةْ³ةDخھ(CH3)2CBr-CH2CH2-BrC(CH3)2£¬¸ù¾فذإد¢¢¢؟ةضھ£¬(CH3)2CBr-CH2CH2-BrC(CH3)2سë¼×±½·¢ةْب،´ْ·´س¦ةْ³ةEخھ
سëنه·¢ةْ1£¬4-¼س³ة·´س¦ةْ³ةCخھ(CH3)2CBr-CH=CH-BrC(CH3)2£¬¸أسذ»ْخïسëاâئّ·¢ةْ¼س³ة·´س¦ةْ³ةDخھ(CH3)2CBr-CH2CH2-BrC(CH3)2£¬¸ù¾فذإد¢¢¢؟ةضھ£¬(CH3)2CBr-CH2CH2-BrC(CH3)2سë¼×±½·¢ةْب،´ْ·´س¦ةْ³ةEخھ £»ب»؛َ¸ù¾فذإد¢¢،؟ةضھ£¬سذ»ْخï
£»ب»؛َ¸ù¾فذإد¢¢،؟ةضھ£¬سذ»ْخï سë
سë ·¢ةْب،´ْ·´س¦ةْ³ة
·¢ةْب،´ْ·´س¦ةْ³ة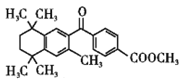 £»
£» شعثلذشجُ¼دآ·¢ةْث®½âةْ³ةFخھ
شعثلذشجُ¼دآ·¢ةْث®½âةْ³ةFخھ £¬زش´ث½â´ً¸أجâ،£
£¬زش´ث½â´ً¸أجâ،£
£¨1£©¶ش¶¼×±½±»ثلذش¸كأجثل¼طرُ»¯خھ¶ش±½¶¼×ثل£¬·´س¦¢ظµؤ·´س¦ہàذحتارُ»¯·´س¦£»
£¨2£©¶ش±½¶¼×ثلسë¼×´¼·¢ةُْ¥»¯·´س¦ةْ³ةB£¬·´س¦¢عµؤ»¯ر§·½³جت½£؛![]() +CH3OH
+CH3OH![]()
![]() +H2O£»
+H2O£»
£¨3£©¸ù¾فزشةد·ضخِ؟ةضھ£¬سذ»ْخïCµؤ½ل¹¹¼ٍت½خھ(CH3)2CBr-CH=CH-BrC(CH3)2£¬زشج¼ج¼ث«¼üخھ¶ش³ئضل½ّذذ·ضخِ؟ةضھ£¬؛ث´إ¹²صٌاâئ×ح¼ضذسذ2¸ِ·ه£»
£¨4£©¸ù¾فذإد¢¢¢؟ةضھ£¬(CH3)2CBr-CH2CH2-BrC(CH3)2سë![]() ·¢ةْب،´ْ·´س¦ةْ³ة
·¢ةْب،´ْ·´س¦ةْ³ة £»·´س¦¢غµؤ»¯ر§·½³جت½£؛(CH3)2CBr-CH2CH2-BrC(CH3)2+
£»·´س¦¢غµؤ»¯ر§·½³جت½£؛(CH3)2CBr-CH2CH2-BrC(CH3)2+![]()
![]()
 +2HBr£»
+2HBr£»
£¨5£©×غةد·ضخِ؟ةضھ£¬سذ»ْخïFµؤ·ض×ست½تاC24H28O2£¬½ل¹¹¼ٍت½خھ £¬؛¬سذµؤ¹ظؤـحإ£؛ج¼ج¼ث«¼ü،¢ôب»ù£»
£¬؛¬سذµؤ¹ظؤـحإ£؛ج¼ج¼ث«¼ü،¢ôب»ù£»
£¨6£©سذ»ْخïAخھ¶ش±½¶¼×ثل£¬ح¬·ضزى¹¹جهآْ×مa،£±½»·ةدµؤز»آب´ْخïسذء½ضض£»b£®¼بؤـ·¢ةْزّ¾µ·´س¦سضؤـ·¢ةْث®½â·´س¦£¬½ل¹¹ضذ؛¬سذHCOO-ب،´ْ»ù£¬¾كجه½ل¹¹بçدآ£؛![]() ،¢
،¢![]() £»
£»
£¨7£©ززد©سëنه¼س³ةةْ³ةBrCH2CH2Br£¬BrCH2CH2Br·¢ةْب،´ْةْ³ةHOCH2CH2OH£¬HOCH2CH2OH±»رُ»¯خھOHCCHO£¬¸ù¾فذإد¢²¢½ل؛دةْ³ةخïµؤ½ل¹¹¼ٍت½؟ةضھ£¬OHCCHOسëCH3CHBrCH3شعMg/H2Oجُ¼دآ·¢ةْ¼س³ة·´س¦ةْ³ة £¬¸أسذ»ْخïشظ·¢ةْدûب¥·´س¦ةْ³ة
£¬¸أسذ»ْخïشظ·¢ةْدûب¥·´س¦ةْ³ة![]() £¬¾كجه؛د³ةآ·دكبçدآ£؛CH2=CH2
£¬¾كجه؛د³ةآ·دكبçدآ£؛CH2=CH2![]() BrCH2CH2Br
BrCH2CH2Br![]() HOCH2CH2OH
HOCH2CH2OH![]() OHC-CHO
OHC-CHO![]()

![]()
![]() ،£
،£

 ذآ»îء¦×ـ¶¯ش±تîدµءذ´ً°¸
ذآ»îء¦×ـ¶¯ش±تîدµءذ´ً°¸ ءْبثح¼تé؟ىہض¼ظئعتî¼ظ×÷زµض£ضف´َر§³ِ°وةçدµءذ´ً°¸
ءْبثح¼تé؟ىہض¼ظئعتî¼ظ×÷زµض£ضف´َر§³ِ°وةçدµءذ´ً°¸،¾جâؤ؟،؟شع3¸ِجه»¾ùخھ2.0Lµؤ؛مبفأـ±صبفئ÷ضذ£¬·´س¦CO2(g)+C(s)![]() 2CO(g) H£¾0·ض±ًشعز»¶¨خآ¶بدآ´ïµ½»¯ر§ئ½؛â×´ج¬،£دآءذثµ·¨صب·µؤتا£¨ £©
2CO(g) H£¾0·ض±ًشعز»¶¨خآ¶بدآ´ïµ½»¯ر§ئ½؛â×´ج¬،£دآءذثµ·¨صب·µؤتا£¨ £©
بفئ÷ | خآ¶ب/K | ئًت¼ت±خïضتµؤء؟/mol | ئ½؛âت±خïضتµؤء؟/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
¢ٌ | 977 | 0.28 | 0.56 | 0 | 0.4 |
¢ٍ | 977 | 0.56 | 0.56 | 0 | x |
¢َ | 1250 | 0 | 0 | 0.56 | y |
A.´ïµ½ئ½؛âت±£¬دٍبفئ÷¢ٌضذشِ¼سC(s)µؤء؟£¬ئ½؛âصدٍزئ¶¯
B.x=0.8£¬y£¾0.4
C.´ïµ½ئ½؛âت±£¬بفئ÷¢َضذµؤCOµؤ×ھ»¯آتذ،سع![]()
D.بôئًت¼ت±دٍبفئ÷¢ٍضذ³نبë0.1molCO2،¢0.2molCO؛ح×مء؟µؤC(s)£¬شٍ·´س¦½«دٍص·´س¦·½دٍ½ّذذ
،¾جâؤ؟،؟زرضھ25،وت±£¬¼¸ضض³£¼ûبُثلµؤKaبçدآ±يثùت¾£؛
µç½âضت | H2C2O4 | CH3COOH | HCN | H2CO3 |
µçہë³£ت£¨molL-1£© | K1=5.6،ء10-2 K2=5.4،ء10-3 | K=1.7،ء10-5 | K=6.2،ء10-10 | K1=4.2،ء10-7 K2=5.6،ء10-11 |
£¨1£©²فثل£¨H2C2O4£©تاز»ضض___£¨جî،°ز»شھ،±،¢،°¶شھ،±،¢،°¶àشھ،±£©بُثل،£25،وت±£¬0.1molL-1µؤNa2C2O4،¢CH3COONa،¢NaCN،¢Na2CO3بـز؛µؤpHسة´َµ½ذ،µؤث³ذٍتا__،£
£¨2£©KHC2O4بـز؛³تثلذش£¬دٍ10mL0.01molL-1µؤH2C2O4بـز؛µخ¼س0.01molL-1KOHبـز؛V(mL)،£»ط´ًدآءذختجâ£؛
¢ظµ±V<10mLت±£¬·´س¦µؤہë×س·½³جت½خھ___،£
¢عµ±V=10mLت±£¬بـز؛ضذ![]() ،¢
،¢![]() ،¢H2C2O4،¢H+µؤإ¨¶بسة´َµ½ذ،µؤث³ذٍخھ__،£
،¢H2C2O4،¢H+µؤإ¨¶بسة´َµ½ذ،µؤث³ذٍخھ__،£
¢غµ±V=amLت±£¬بـز؛ضذہë×سإ¨¶بسذبçدآ¹طدµ£؛c(K+)=2c(![]() )+c(
)+c(![]() )£»µ±V=bmLت±£¬بـز؛ضذہë×سإ¨¶بسذبçدآ¹طدµ£؛c(K+)=c(
)£»µ±V=bmLت±£¬بـز؛ضذہë×سإ¨¶بسذبçدآ¹طدµ£؛c(K+)=c(![]() )+c(
)+c(![]() )+c(H2C2O4)£»شٍa__b£¨جî،°<،±،°=،±»ٍ،°>،±£©.
)+c(H2C2O4)£»شٍa__b£¨جî،°<،±،°=،±»ٍ،°>،±£©.