题目内容
15.你认为下列数据可信的是( )| A. | 某溶液中溶质的质量分数超过100% | B. | 某常见气体的密度为1.8g/cm3 | ||
| C. | 用10ml量筒量取5.23ml浓硫酸 | D. | 用托盘天平称得氯化钠 5.0g |
分析 A.溶液由溶质与溶剂构成,溶质质量小于溶液质量;
B.气体的密度应小于水的密度;
C.量筒精确度为0.1mL;
D.托盘天平的精确度为0.1g.
解答 解:A.溶液由溶质与溶剂构成,溶质质量小于溶液质量,故溶质的质量分数小于100%,故A错误;
B.通常条件下,水的密度约是1g/mL,气体的密度应小于水的密度,故B错误;
C.量筒精确度为0.1mL,用10ml量筒量取5.2mL浓硫酸,故C错误;
D.托盘天平的精确度为0.1g,则用托盘天平称得氯化钠 5.0g,故D正确.
故选D.
点评 本题考查溶液浓度有关计算、仪器的使用等,侧重对学生综合能力的考查,题目难度不大.

练习册系列答案
相关题目
6.下列关于胶体的叙述不正确的是( )
| A. | 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 | |
| B. | 光线透过胶体时,胶体发生了丁达尔现象 | |
| C. | 用渗析的方法净化胶体时,半透膜只允许较小的分子、离子通过 | |
| D. | 胶体粒子具有较大的表面积,能吸附阳离子或阴离子,故在电场的作用下会产生电泳现象 |
3.室温下,设1LpH=6的AlCl3溶液中,由水电离出的H+物质的量为n1;1LpH=6的HCl溶液中,由水电离出的H+物质的量为n2.则$\frac{{n}_{1}}{{n}_{2}}$的值是( )
| A. | 1 | B. | 100 | C. | 1000 | D. | 10000 |
10.下列说法正确的是( )
| A. | 由H原子形成1molH-H键要吸收热量 | |
| B. | C(石墨,s)═C(金刚石,s)△H=+1.9 kJ/mol,则可判定金刚石比石墨稳定 | |
| C. | 500℃、30 MPa下,0.5 mol N2(g)和1.5 mol H2(g)反应生成NH3(g)放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知Ni(CO)4(s)=Ni(s)+4CO(g)△H=Q kJ•mol-1,则Ni(s)+4CO(g)=Ni(CO)4(s)△H=-Q kJ•mol-1 |
20.下列实验,所选装置合理的是
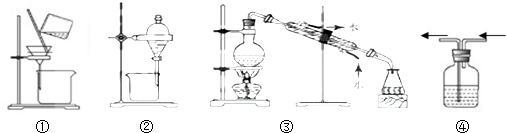 ( )
( )
 ( )
( )| A. | 提纯含NaCl的氢氧化铁胶体用装置① | |
| B. | 分离碘的四氯化碳溶液用② | |
| C. | 分离NaCl的酒精溶液用装置③ | |
| D. | 除去Cl2中的HCl气体用装置④ |
7.下列属于吸热反应的是( )
| A. | 镁条在空气中燃烧 | B. | 盐酸与NaOH溶液反应 | ||
| C. | 酒精在空气中燃烧 | D. | Ba(OH)2?8H2O晶体与NH4Cl晶体反应 |
4.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 标况下,22.4 L水中氢原子原子数大于1NA | |
| B. | 1LpH=1的醋酸溶液中H+数目为0.1NA | |
| C. | 10g46%的甲酸(HCOOH)水溶液中所含氧原子数为0.5 NA | |
| D. | 1molFe溶于稀硝酸过程中电子转移数为2 NA |
5.下列说法正确的是( )
| A. | 固体硝酸钾不导电,所以硝酸钾是非电解质 | |
| B. | 石墨能导电,所以石墨是电解质 | |
| C. | CO2的水溶液能导电,故CO2是电解质 | |
| D. | 盐酸能导电,故氯化氢是电解质 |