题目内容
【题目】25℃时,在50 mL 0.1 mol·L1的NaOH溶液中逐滴加入0.2 mol·L1的醋酸,溶液pH随所加醋酸的体积变化曲线如图。下列说法正确的是
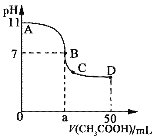
A.在A、B之间任意一点都满足:c(Na+)>c(CH3COO)>c(OH)>c(H+)
B.在B点,a>25,且c(Na+)=c(CH3COO)=c(OH)=c(H+)
C.在C点:c(Na+)>c(CH3COO)>c(H+)>c(OH)
D.在D点:c(OH) +c(Na+)=c(CH3COOH)+c(H+)
【答案】D
【解析】选项A,由图像可知在A、B之间,靠近A点附近对应的溶液中NaOH过量,溶液中c(OH)>c(CH3COO),由此可判断A项错误。选项B,在B点,因溶液呈中性则醋酸略过量,a>25,但此时c(CH3COO)= c(Na+)>c(H+)=c(OH),错误。选项C,在C点醋酸过量,则:c(CH3COO)>c(Na+)>c(H+)>c(OH),错误。选项D,用物料守恒:c(CH3COO)+c(CH3COOH)=2c(Na+)减去电荷守恒:c(OH)+ c(CH3COO)= c(Na+)+c(H+)即可得:c(OH) + c(Na+)=c(CH3COOH)+ c(H+),正确。

【题目】镁、铜等金属离子是人体内多种酶的辅因子。
(1)Cu位于元素周期表第四周期,铜原子核外电子有____种不同的运动状态,Cu+的核外电子排布式为________。
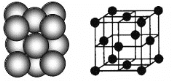
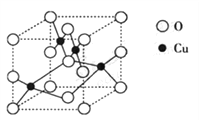
(2)下图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴、阳离子个数比为______。
(3)Mg是第三周期元素,该周期部分元素氟化物的熔点下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1266 | 1534 | 183 |
解释表中氟化物熔点差异的原因:___________________________。