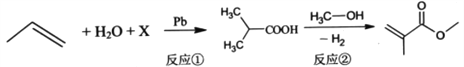
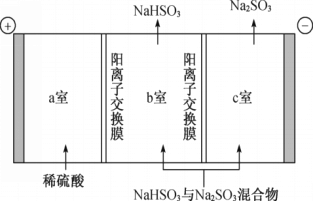
题目内容
【题目】下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+ ![]() AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
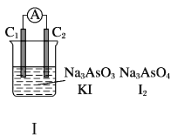
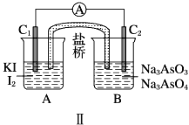
下列叙述中正确的是
A. 甲组操作时,电流表(A)指针发生偏转
B. 甲组操作时,溶液颜色变浅
C. 乙组操作时,C2作正极
D. 乙组操作时,C1上发生的电极反应为I2+2e-=2I-
【答案】D
【解析】
A、甲组操作时,两个电极均为碳棒,不发生原电池反应,电流表指针不发生偏转,故A错误;
B、根据题中所给反应,生成I2,溶液颜色加深,故B错误;
C、根据反应方程式,以及乙组操作,As的化合价由+3价→+5价,化合价升高,即C2为负极,故C错误;
D、根据C选项分析,C1电极反应式为I2+2e-=2I-,故D正确。

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
【题目】任何物质的水溶液都存在水的电离平衡,其电离方程式可表示为:![]() 。下表是不同温度下水的离子积数据:
。下表是不同温度下水的离子积数据:
温度(℃) | 25 |
|
|
水的离子积常数 |
| a |
|
完成下列填空:
(1)25℃时,向100mL纯水中加入0.01mol的![]() 固体,________(选填“促进”或“抑制”)了水的电离平衡,所得溶液呈________性(选填“酸”、“碱”或“中”),原因是(用离子反应方程式表示)________________________。
固体,________(选填“促进”或“抑制”)了水的电离平衡,所得溶液呈________性(选填“酸”、“碱”或“中”),原因是(用离子反应方程式表示)________________________。
(2)若![]() ,则a________
,则a________![]() (选填“
(选填“![]() ”、“
”、“![]() ”或“=”),理由是____________。
”或“=”),理由是____________。
(3)![]() ℃时,测得纯水的
℃时,测得纯水的![]() ,则
,则![]() ________mol/L;该温度下某盐酸溶液的
________mol/L;该温度下某盐酸溶液的![]() ,该溶液的
,该溶液的![]() ________mol/L。
________mol/L。
(4)![]() ℃时,0.01mol/L的NaOH溶液的
℃时,0.01mol/L的NaOH溶液的![]() ________。
________。