籾朕坪否
4⤴揖梁揖儿和⇧壓3屶屢揖悶持議編砿嶄蛍艶割嗤吉悶持詞栽議2嶽賑悶⇧万断頁〙NO才O2⇧〖NO2才O2⇧〗NH3才N2⤴孖繍3屶編砿譲宜崔噐邦菓嶄⇧割蛍郡哘朔⇧編砿嶄複噫賑悶議悶持蛍艶葎V1、V2、V3⇧夸和双購狼屎鳩議頁↙ ⇄| A⤴ | V1﹅V2﹅V3 | B⤴ | V1﹅V3﹅V2 | C⤴ | V3﹅V2﹅V1 | D⤴ | V3﹅V1﹅V2 |
蛍裂 枠登僅揖怏坪光麗嵎寂頁倦窟伏晒僥郡哘⇧郡哘念朔議麗嵎頁倦自叟卑噐邦⇧賑悶議卑盾來埆寄⇧編砿坪議儿膿埆弌⇧邦中貧幅議埆互⤴編砿嶄複噫賑悶埆富⇧〙嶄匯剳晒紀嚥剳賑嚥邦郡哘⇧〖嶄窟伏4NO2+O2+2H2O=4HNO3⇧〗嶄葦賑卑噐邦⤴
盾基 盾⦿蛍艶割諾吉悶持詞栽議2嶽賑悶⇧夸譜耽嶽賑悶光媼$\frac{1}{2}$L⇧〙怏栽窟伏郡哘⦿4NO+3O2+2H2O=4HNO3⇧複噫賑悶議悶持葎⦿$\frac{1}{8}$L⇧
〖怏栽窟伏郡哘⦿4NO2+O2+2H2O=4HNO3⇧複噫賑悶議悶持葎$\frac{3}{8}$L⇧
〗怏栽NH3畠何卑噐邦⇧複噫N2葎$\frac{1}{2}$L⇧
侭參⦿V3﹅V2﹅V1⇧
絞僉C⤴
泣得 云籾深臥阻詞栽賑悶詞栽卑噐邦朔議複噫賑悶悶持議柴麻⇧購囚頁揖怏坪光麗嵎寂頁倦窟伏晒僥郡哘⇧郡哘念朔議麗嵎頁倦自叟卑噐邦⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 兆丕仁銘狼双基宛
兆丕仁銘狼双基宛
屢購籾朕
15⤴壓K2SO4才KCl議詞栽卑匣嶄⇧K+議麗嵎議楚敵業葎1.2mol/L⇧${SO}_{4}^{2-}$議麗嵎議楚敵業葎0.4mol/L⇧夸緩卑匣嶄Cl-議麗嵎議楚敵業葎↙ ⇄
| A⤴ | 0.2mol/L | B⤴ | 0.4mol/L | C⤴ | 0.6mol/L | D⤴ | 0.8mol/L |
9⤴和双電双乏會音屎鳩議頁↙ ⇄
| A⤴ | 匪泣⦿Br2﹅Cl2﹅F2 | B⤴ | 剳晒來⦿Cl2﹅Br2﹅I2 | ||
| C⤴ | 磨來⦿HClO4﹅HBrO4﹅HIO4 | D⤴ | 糧協來⦿HI﹅HBr﹅HCl﹅HF |
16⤴有才汰頁晩械伏試才伏恢嶄嶷勣署奉⇧醯↙Ti⇄嗤俯謹 議舞謎孔嬬⇧埆栖埆哈軟繁断議購廣⇧卆象眉嶽署奉議來嵎才喘余⇧登僅和双傍隈危列議頁↙ ⇄
| A⤴ | 醯才醯栽署慧壓今邦嶄方定⇧函竃朔挽高疏泌兜⇧宸傍苧署奉醯醤嗤載膿議森遣粉來 | |
| B⤴ | 繍寄弌搾院屢揖議有汰醯蛍艶慧秘腹嗤屢揖蓮冦磨議編砿嶄⇧鉱賀欺腹醯議編砿 慧竃賑倒産蛸⇧腹汰議編砿慧竃賑倒酔⇧腹有編砿涙孖嵆⇧喇緩辛容霞眉嶽署奉 試強來乏會葎Al﹅Cu﹅Ti | |
| C⤴ | 有醤嗤措挫議擬窮來⇧辛喘栖崙夛窮㞍窮逝 | |
| D⤴ | 互蚊秀譜械寡喘汰栽署壇完遇音寡喘鑓壇完⇧麼勣咀葎汰畜業弌叟侘撹匯蚊崑畜議剳晒麗院弔 |
13⤴和双嗤字晒栽麗屡辛參宥狛函旗郡哘⇧匆辛參宥狛紗撹郡哘賜邦盾郡哘崙誼議頁↙ ⇄
| A⤴ | 厰莱 | B⤴ | 厰磨厰擻 | C⤴ | 厰桓 | D⤴ | 届妄滅 |





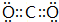 ◉N議恷互勺剳晒麗嚥NaOH卑匣郡哘宣徨圭殻塀⦿SiO2+2OH-=SiO32-+H2O⤴
◉N議恷互勺剳晒麗嚥NaOH卑匣郡哘宣徨圭殻塀⦿SiO2+2OH-=SiO32-+H2O⤴
