题目内容
11.设NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,H2的气体摩尔体积约为22.4L | |
| B. | 标准状况下,22.4L的CO2和O2组成的混合物中,含氧原子数为2NA | |
| C. | 1mol/L CaCl2溶液中含有的氯离子数目为2NA | |
| D. | 18gNH4+中含有10NA个质子 |
分析 A、气体摩尔体积的单位为L/mol;
B、二氧化碳和氧气中均含2个氧原子;
C、溶液体积不明确;
D、求出铵根离子的物质的量,然后根据1mol铵根离子中含11mol质子来分析.
解答 解:A、气体摩尔体积的单位为L/mol,只与状态有关,即标况下气体摩尔体积为22.4L/mol,故A错误;
B、标况下22.4L二氧化碳和氧气混合气体的物质的量为1mol,而二氧化碳和氧气中均含2个氧原子,故1mol混合气体中氧原子为2NA个,故B正确;
C、溶液体积不明确,故溶液中的氯离子的个数无法计算,故C错误;
D、18g铵根离子的物质的量为1mol,而1mol铵根离子中含11mol质子,即11NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
2.在四个不同的容器中,在不同的条件下进行合成氨反应.根据在相同时间内测定的结果判断,生成氨的速率最快的是( )
| A. | υ(H2)=0.1 mol•L-1•s-1 | B. | υ(N2)=0.2 mol•L-1•min-1 | ||
| C. | υ(NH3)=0.15 mol•L-1•min-1 | D. | υ(H2)=0.3 mol•L-1•min-1 |
19.平衡体系 CaCO3(s)?CaO(s)+CO2(g) 中仅含碳酸钙、氧化钙及二氧化碳气体.某时刻保持 温度不变,往恒容密闭容器中再通一定量 CO2 气体,体系重新达到平衡,下列说法正确的是( )
| A. | 平衡常数减小 | B. | CaO 的量不变 | C. | CO2浓度不变 | D. | CO2 浓度增大 |
3.下列反应中,属于氧化还原反应的是( )
| A. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | B. | CuCl2+2 NaOH═Cu(OH)2↓+2NaCl | ||
| C. | FeO+2 HCl═FeCl2+H2O | D. | 2Al(OH)3 $\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3 H2O |
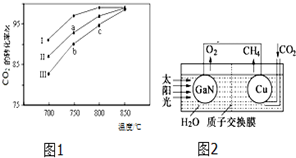 二氧化碳的捕集、利用与封存(CCUS)是我国能源领域的一个重要战略方向,CCUS或许发展成一项重要的新兴产业.利用废气中的 CO2为原料可制取甲醇,在恒容密闭容器中,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).
二氧化碳的捕集、利用与封存(CCUS)是我国能源领域的一个重要战略方向,CCUS或许发展成一项重要的新兴产业.利用废气中的 CO2为原料可制取甲醇,在恒容密闭容器中,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).