题目内容
19.平衡体系 CaCO3(s)?CaO(s)+CO2(g) 中仅含碳酸钙、氧化钙及二氧化碳气体.某时刻保持 温度不变,往恒容密闭容器中再通一定量 CO2 气体,体系重新达到平衡,下列说法正确的是( )| A. | 平衡常数减小 | B. | CaO 的量不变 | C. | CO2浓度不变 | D. | CO2 浓度增大 |
分析 根据再充入CO2,平衡逆向移动,CaO 的量变小,K=c(CO2),平衡常数仅与温度有关来判断.
解答 解:CaCO3(s)?CaO(s)+CO2(g),K=c(CO2),再充入CO2,平衡逆向移动,CaO 的量变小,但因为温度没变,则K=c(CO2)不变,所以CO2浓度不变,
故选:C.
点评 本题主要考查了平衡移动及其平衡常数的表达式及其影响因素,难度不大,抓住平衡常数仅与温度有关即可解题;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列物质能导电,但属于电解质的是( )
| A. | 纯净的硫酸 | B. | KNO3 溶液 | C. | NH4HCO3固体 | D. | 熔融的KCl |
7.下列溶液一定呈酸性的是( )
| A. | pH=6.8的溶液 | |
| B. | 常温下,由水电离的OH-离子浓度为1×10-13 mol/L | |
| C. | 加入酚酞,不显红色的溶液 | |
| D. | 常温下,溶液中的H+离子浓度为5×10-7 mol/L |
14.下列事实不能用勒夏特列原理解释的是( )
| A. | 光照新制的氯水时,溶液的 pH 逐渐减小 | |
| B. | 对 CO(g)+NO2(g)?CO2(g)+NO(g),平衡体系增大压强可使颜色变深 | |
| C. | 高压下有利于提高合成氨的产率 | |
| D. | 可用浓氨水和氢氧化钠固体快速制氨 |
11.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,H2的气体摩尔体积约为22.4L | |
| B. | 标准状况下,22.4L的CO2和O2组成的混合物中,含氧原子数为2NA | |
| C. | 1mol/L CaCl2溶液中含有的氯离子数目为2NA | |
| D. | 18gNH4+中含有10NA个质子 |
8.下列说法正确的是( )
| A. | 在Na2CO3溶液中:c(Na+):c(CO32-)=2:1 | |
| B. | 在25℃时,无论是酸性、碱性或中性溶液中,其c(H+)和c(OH-)的乘积都等于1×10-14 | |
| C. | 0.1mol/L的KOH溶液和0.1mol/L氨水中,c(OH-)相等 | |
| D. | 原电池的正极所发生的反应是氧化反应 |

 为了证明铜与稀硝酸反应产生一氧化氮,某校同学设计了一个 实验,其装置如图所示(加热装置和固定装置均已略去).
为了证明铜与稀硝酸反应产生一氧化氮,某校同学设计了一个 实验,其装置如图所示(加热装置和固定装置均已略去).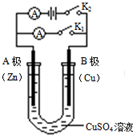 如右图所示,请按要求回答下列问题.
如右图所示,请按要求回答下列问题.