��Ŀ����
����Ŀ��(M��)�о�̼�������仯�����ת�����ڻ����ĸ������ش����塣������ԭ������NOx��ת�����£�NO![]() NO2
NO2![]() N2
N2
��֪��NO(g)+O3(g)==NO2(g)+O2(g) ��H��-200.9kJ��mol-1
2NO(g)+O2(g)==2NO2(g) ��H��-2116.2kJ��mol-1
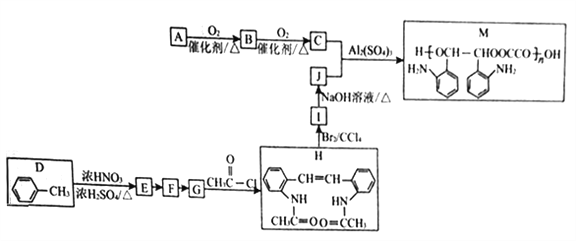
(1)��ӦI���Ȼ�ѧ����ʽΪ_________________��
(2)�������뽫CO�����з�Ӧ��ȥ:2CO(g)==2C(s)+O2(g) ��H >0������Ϊ�������ܷ�ʵ�ֲ�˵�����ɣ�_____________________��
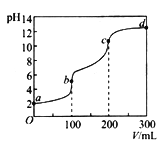
(3)һ�������£�CO�����ĩ״�����������������ɼ����ơ���֪����ʱ������ĵ���ƽ�ⳣ��Ka= l.70��10-4����20 mL 0.1 mol/L�ļ�������Һ�еμ�10mL 0.1 mol/L�����ᣬ���Һ��_____(��ᡱ����ԣ���Һ������Ũ�ȴӴ�С��˳��Ϊ_____________��
(4)����̿Ҳ�����ڴ�������β���е�NO����2 L�����ܱ������м���0.1000 mol NO��2.030 mol�������̿������A��B�������壬�ڲ�ͬ�¶��²��ƽ����ϵ�и����ʵ����ʵ������±���
�������̿/mol | NO/mol | A/mol | B/mol | |
200�� | 2.000 | 0.040 0 | 0.030 0 | 0.030 0 |
335�� | 2.005 | 0.050 0 | 0.025 0 | 0.025 0 |
�ٸ÷�Ӧ������ӦΪ_________(����ȡ����ȡ�)��Ӧ��
��200��ʱ��ƽ���������������ٳ���0.100 0 mol NO���ٴ�ƽ���NO�İٷֺ�����__________(�������С�����䡱)��
�ۼ��㷴Ӧ��ϵ��335��ʱ��ƽ�ⳣ��_______________��
(5)CO2�Ĵ��������ж��֣�������CO2����ͨ��ʯ�����г�ַ�Ӧ���ﵽƽ������Һ��c(OH-)=c mol/L����c(CO32-)=_____ mol��L-1(�ú�a��b��c�Ĵ���ʽ��ʾ)��(��֪Kap(CaCO3)=a��Kap[Ca(OH)2]=b)
���𰸡� 3NO(g)+O2(g)==3NO2(g) ��H=-317.1 kJ/mol ��,�÷�Ӧ���������ؼ��ķ�Ӧ�����ݡ�S. ��G>0����Ӧ�����Է��J��(2�֣�ͬʱ���жϺ����ɲŸ���) �� c(Na+)>c(HCOO-)>c(Cl-)>c(H+)>c(OH-) ���� ���� 0.25 ![]()
��������(1)��Ӧ��NO(g)��O3(g)���ݸ�˹���ɣ���NO(g)+O3(g)�TNO2(g)+O2(g)��H=-200.9kJ/mol����2NO(g)+O2(g)�T2NO(g)��H=-116.2kJ/mol����Ŀ�귴Ӧ�ķ�Ӧ�ȵ��ڢ�+�ڣ�����I���Ȼ�ѧ����ʽΪ3NO(g)+O3(g)�T3NO2(g)��H=-317.1kJmol-1��
(2)���ݡ�G=��H-T��S�жϷ�Ӧ�ܷ��Է����У������G��0����Ӧ���Է����У���G��0����Ӧ�����Է����У�2CO(g)=2C(s)+O2(g)���÷�Ӧ���������ؼ��ķ�Ӧ������G=��H-T��S��G��0������ʵ�֣�
(3)��20mL0.1mol/L�ļ�������Һ�еμ�10ml0.1mol/L�����ᣬ�õ������ʵ���Ũ�ȵļ��ᡢ�����ƺ��Ȼ��ƵĻ��Һ���Լ���ĵ���Ϊ������Һ�����ԣ���Һ������Ũ�ȴӴ�С��˳��Ϊc(Na+)��c(HCOO-)��c(Cl-)��c(H+)��c(OH-)��
(4)���¶�����ƽ�������ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
����200��ʱ�������ʵ�����ϵ��֪����Ӧ����ʽΪ��2NOA+B����������ļ�������ȣ���ƽ���������������ٳ���0.1molNO���൱������ѹǿ��ƽ�ⲻ�ƶ�������NO�İٷֺ��������䣻
��ƽ�ⳣ������ƽ��ʱ�������Ũ����֮�����Ϸ�Ӧ��Ũ����֮��������K= =0.25��
=0.25��
(5)������CO2����ͨ��ʯ�����г�ַ�Ӧ���ﵽƽ������ķ�ӦΪ��Ca2++CO32-CaCO3+2OH-��ƽ�ⳣ��K=![]() ���ﵽƽ������Һc(OH-)=cmolL-1����c(CO32-)=
���ﵽƽ������Һc(OH-)=cmolL-1����c(CO32-)=![]() mol/L��
mol/L��

����Ŀ��ijУ��ѧ��ȤС��̽��SO2��һЩ���ʡ�
[̽��һ]��SO2�ܷ�BaCl2��Һ���ա�
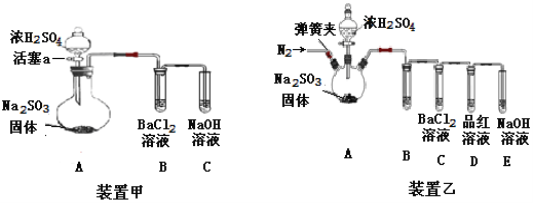
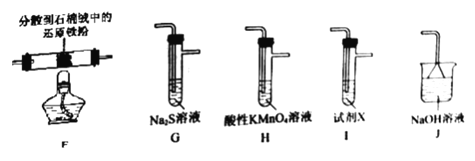
�ס�����ͬѧ�ֱ��������װ�ü�װ���ҽ���̽��
�ס�����ͬѧʵ��ʱ�۲쵽�������е��������£�
A | B | C | D | |
װ�ü��е����� | Na2SO3�������������.ƿ�а��� | ��ɫ���� | ----- | ------ |
װ�����е����� | Na2SO3�������������.ƿ�а��� | ������ | ������ | Ʒ����ɫ |
�ش��������⣺
��1����ͬѧ��������ʵ��ȷ֤��B�а�ɫ������BaSO4.��ͬѧ�ĺ���ʵ�������____
��2����ͬѧ����װ�ü��в���BaSO4�Ŀ���ԭ���У�
��A�в����İ��������������������B����BaCl2��Һ��Ӧ����BaSO��������
��________________________�������ӷ���ʽ��ʾ����
��3��װ������B����ʢ�Լ���___����ͬѧ�ڵμ�Ũ����֮ǰ�IJ�����___________
��4��ͨ������ʵ�飬�ó��Ľ�����________________________
[̽����]��SO2��FeCl3��Һ�ķ�Ӧ
�������ϣ���Fe(HSO3)2+����Ϊ����ɫ�������Խ�Fe3+��ԭΪFe2+��������Fe(HSO3)2+���ӵķ�ӦΪ���淴Ӧ��ʵ�鲽��Ϊ��
����I | ��5mL1mol��L-1 FeCl3��Һ��ͨ��SO2���壬��Һ������Ϊ����ɫ����3 min����Һ��ɫ��Ϊdz��ɫ�� |
����II | ��5mL�������Ƶ�1mol��L-1 FeCl3��Һ����Ũ�����ữ����ͨ��SO2���壬��Һ������Ϊ����ɫ�������Ӻ�����Һ��ɫ���dz��ɫ�� |
�ش���������:
��5����SO2ͨ�뵽FeCl3��δ�������ữ����Һ������ʱ��ͬѧ�ǹ۲쵽����������Һ���ػ�ɫ��ɺ���ɫ��û�й۲쵽������������Һ����12Сʱ����Һ�ű��dz��ɫ������Һ���ػ�ɫ��ɺ���ɫ��ԭ����_________��д����Һ�ɺ���ɫ��Ϊdz��ɫʱ������Ӧ�����ӷ���ʽ___________
��6��ͨ��ʵ���֪_____��________������dz��ɫ���ֵ�ʱ�䡣