题目内容
【题目】下列水解方程式的书写不正确的是( )
A.NH4++H2O![]() NH3·H2O+H+
NH3·H2O+H+
B.S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C.CH3COONa+H2O![]() CH3COOH+NaOH
CH3COOH+NaOH
D.MgCO3 + H2O![]() Mg(OH)2 + CO2
Mg(OH)2 + CO2
【答案】B
【解析】
水解离子反应中弱酸或弱碱离子结合水电离生成的氢离子或氢氧根离子生成弱电解质,以此分析。
A.铵根离子水解生成一水合氨和氢离子NH4++H2O![]() NH3·H2O+H+,则属于水解离子反应,选项A正确;
NH3·H2O+H+,则属于水解离子反应,选项A正确;
B.硫离子水解分步进行,以第一步为主,不能一步完成,应为S2-+H2O![]() HS-+OH-、HS-+H2O
HS-+OH-、HS-+H2O![]() H2S+OH-,选项B错误;
H2S+OH-,选项B错误;
C.醋酸钠水解产生醋酸和氢氧化钠CH3COONa+H2O![]() CH3COOH+NaOH,水解方程式书写正确,选项C正确;
CH3COOH+NaOH,水解方程式书写正确,选项C正确;
D.加热条件下碳酸镁水解产生更难溶的氢氧化镁,同时生成二氧化碳气体MgCO3 + H2O![]() Mg(OH)2 + CO2,属于水解反应,选项D正确;
Mg(OH)2 + CO2,属于水解反应,选项D正确;
答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】甲胺(CH3NH2)是合成太阳能敏化剂的原料。一定温度下,在三个体积均为2.0 L的恒容密闭容器中按不同方式投入反应物,发生反应CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g),测得有关实验数据如下:
容器编号 | 温度/K | 起始物质的量(mol) | 平衡物质的量mol | ||||
CH3OH | NH3 | CH3NH2 | H2O | CH3NH2 | H2O | ||
I | 530 | 0.40 | 0.40 | 0 | 0 | 0.30 | |
II | 530 | 0.80 | 0.80 | 0 | 0 | ||
III | 500 | 0 | 0 | 0.20 | 0.20 | 0.16 | |
下列说法正确的是( )
A. 正反应的平衡常数K(Ⅰ)=K(Ⅱ)<K(Ⅲ)
B. 达到平衡时,体系中c(CH3OH)关系:2c(CH3OH,Ⅰ)>c(CH3OH,Ⅱ)
D. 530K时,若起始向容器Ⅰ中充入CH3OH 0.10 mol、NH3 0.15 mol、CH3NH2 0.10 mol、H2O 0.10 mol,则反应将向逆反应方向进行
【题目】Ⅰ.25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11` | 3.0×10-8 |
请回答下列问题:
(1)写出碳酸的第一级电离方程式:________。
(2)物质的量浓度相同的三种溶液:a.CH3COONa b.NaHCO3 c.NaClO
三种溶液的pH由小到大排列的顺序是___<___< ___(用编号填写)
(3)写出向NaClO溶液中通入少量CO2的化学方程式________。
Ⅱ.(4)碳酸钠溶液呈碱性的原因是:______。(写出离子方程式)。0.01mol/L Na2CO3溶液的pH____0.1mol/LNa2CO3溶液的pH。(填“>”或“<”或“==”)
(5)浓度均为0.1mol/L的①CH3COONa溶液②NH4Cl溶液③稀HCl④Na2SO4溶液按pH由大到小的排列顺序为____
(6)打开无水FeCl3的试剂瓶,常冒出许多“白烟”,发生反应的化学方程式为________
【题目】(11分)某课外小组设计的实验室制取乙酸乙酯的装置如图14-2所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
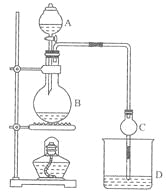
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H ②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用是 ;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式: 。
(2)球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束后D中的现象是 .
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出 (填物质名称);再加入(此空从下列选项中选择,填编号) ,然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。
A.五氧化二磷 | B.碱石灰 | C.无水硫酸钠 | D.生石灰 |