��Ŀ����
����Ŀ��ijѧϰС��ͨ�������ʵ��һ��ʵ�����̽��ijЩ��ѧ���ۣ�
��1��ʵ��һ���Է�Ӧ2Fe3++2I��=2Fe2++I2Ϊ���� ̽���÷�Ӧ�Ƿ�Ϊ���淴Ӧ��
ʵ�鷽������KI��Һ�еμ�3mLFeCl3��Һ�������Һ��
�ȷֵ��ס��ҡ�����֧�Թ��У����Թܼ��еμӵ���
��Һ�����Թ����еμ�KSCN��Һ����ͼ��ʾ��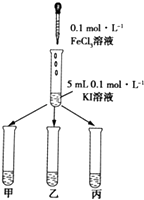
���Թܼ��г�������
���Թ��г�������
��˵���÷�ӦΪ���淴Ӧ��
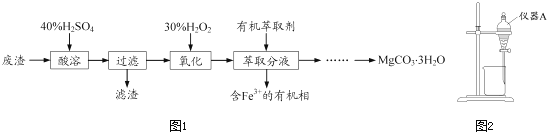
��2��ʵ�����ʵ�����Ʊ�CO2�ķ�Ӧ��ʵ������е����ݼ������Ϣ���±���
��� | ��Ӧ�¶�/�� | C��HCl��/molL��1 | V��HCl��/mL | 10g̼��Ƶ���״ | t/min |
�� | 20 | 2 | 10 | ��״ | t 1 |
�� | 20 | 4 | 10 | ��״ | t 2 |
�� | 20 | 2 | 10 | ��ĩ | t 3 |
�� | 40 | 2 | 10 | ��ĩ | t 4 |
�� | 40 | 4 | 10 | ��ĩ | t5 |
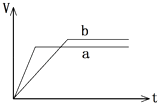
��t��ʾ�ռ���ͬ״���������Ϊa mL CO2�����ʱ���
��i���ɱ����е���Ϣ��֪ʵ�����Ŀ����̽��
��ii��ʵ��ٺ�ʵ�����̽���Ըû�ѧ��Ӧ���ʵ�Ӱ�죬���������е���Ϣ��֪���Ըû�ѧ��Ӧ���ʵ�Ӱ�����ػ���
��iii���ռ�a mL CO2�����ʱ�����ٵ�ʵ��������ʵ����ţ�
���𰸡�
��1��������Ѫ��ɫ
��2��Ӱ�컯ѧ��Ӧ���ʵ����أ�Ũ�ȣ��¶ȡ��Ӵ��������
���������⣺��1����֤����Ӧ2Fe3++2I��=2Fe2++I2Ϊ���淴Ӧ��Ҫ֤����Һ��ͬʱ���������Ӻ͵ⵥ�ʣ���KI��Һ�еμ�3mLFeCl3��Һ�������Һ���ȷֵ��ס��ҡ�����֧�Թ��У����Թܼ��еμӵ�����Һ�����Թ����еμ�KSCN��Һ�����Թܼ��г�����ɫ֤���ⵥ�ʴ��ڣ����Թ��г���Ѫ��ɫ��Һ֤���������ӣ�˵����Ӧ�ǿ��淴Ӧ�����Դ��ǣ���ɫ��Ѫ��ɫ����2����i��ͼ�����ݷ�����֪���٢ڢۢܢ���ʵ��Ŀ����̽��Ӱ�컯ѧ��Ӧ���ʵ����أ���Ҫ���¶ȡ�Ũ�ȡ��Ӵ�����Ի�ѧ��Ӧ���ʵ�Ӱ�죬�ı�һ���������Ի�ѧ��Ӧ����Ӱ�죬�ɱ����е���Ϣ��֪ʵ�����Ŀ����̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�
���Դ��ǣ�Ӱ�컯ѧ��Ӧ���ʵ����أ���ii��ʵ��ٺ�ʵ���������Ũ�Ȳ�ͬ����������ͬ��̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬��Ũ���⣬ͼ�����¶ȡ��Ӵ����Ҳ��Ӱ�컯ѧ��Ӧ���ʣ�
���Դ��ǣ�Ũ�ȣ� �¶ȡ��Ӵ��������iii������ʵ�������֪�Ի�ѧ��Ӧ����Ӱ�������¶����ߣ��¶�Խ�߷�Ӧ����Խ�죬��Ӧ��Ҫ��ʱ��Խ�̣��Ӣܢ���ѡ�ڢ���ʵ��������Ũ�ȴ�Ӧ���ʿ�����ʱ��̣�
���Դ��ǣ��ݣ�

 ��ѧȫ��������ѵ��ϵ�д�
��ѧȫ��������ѵ��ϵ�д�����Ŀ������ΪԪ�����ڱ��е�һ���֣��û�ѧʽ��Ԫ�ط��Żش��������⣺
| ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
�� | �� | �� | �� | |||||
�� | �� | �� | �� | �� | �� | |||
�� | �� | �� |
��1���������γ��������������Ԫ������дԪ�����ƣ�����Ԫ����Ԫ�����ڱ��е�λ���� �� д����Ԫ�ض�Ӧ���������������Ʒ�Ӧ�Ļ�ѧ����ʽ ��
��2���٢ڢ��У�����������Ӧ��ˮ���������ǿ���� �� ��д��ѧʽ�� �����Ӧ����̬�⻯����ȶ��ԴӴ�С��˳���� �� ���û�ѧʽ��ʾ��
��3��Ԫ�آߵ��⻯�����ʽΪ �� ���⻯��������ۺ����ᷴӦ���ɵĻ������к��еĻ�ѧ�������� �� �������������ӡ����ۡ���
��4���ж�Ԫ�آܺ͢��Ӧ�ij������������Ե�ǿ�����û�ѧʽ��ʾ�������û�ѧ����ʽ��������жϣ� ��