题目内容
(1)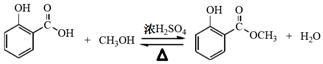 (2分);
(2分);
(2)水浴加热(1分) 反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率 (2分)
(3)蒸馏(1分)
(4)水杨酸(1分) 不可以(1分) 在氢氧化钠溶液中水杨酸甲酯发生水解(1分)
(5)取少量晶体于试管中,加蒸馏水溶解,滴加NaHCO3溶液,若出现无色气泡则含水杨酸(答案合理即可)(2分) 55%(2分)
解析试题分析:(1)制备冬青油的化学方程式为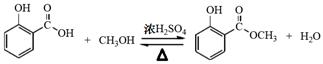 (2分)
(2分)
(2)制备冬青油时,85—95℃最合适的加热方法是水浴加热;实验中加入甲苯作带水剂的目的是反应产生的水从反应体系中分离开来,使得平衡向右移动,同时可以减少甲醇的用量,从而提高反应的产率;
(3)因为甲醇的沸点低,分离甲醇的操作是蒸馏;
(4)用碳酸氢钠溶液洗涤主要除去的杂质是酸性物质水杨酸;NaOH不可以做洗涤剂,因为在氢氧化钠溶液中水杨酸甲酯发生水解;
(5)检验产品中是否含有水杨酸的化学方法是取少量晶体于试管中,加蒸馏水溶解,滴加NaHCO3溶液,若出现无色气泡则含水杨酸(答案不唯一);6.9 g (0.05 mol)水杨酸应得到0.05mol水杨酸甲酯,即7.6g,产品的质量为4.2 g,故所得水杨酸甲酯的产率为55%。
考点:化学实验设计与评价。

练习册系列答案
相关题目
如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是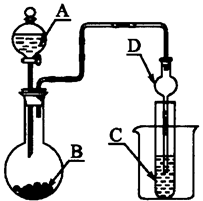
| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液不褪色 |
| B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊 |
| C.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色 |
| D.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀 |
(14分)草酸是一种重要的化工原料,广泛用于药物生产、高分子合成等工业,草酸晶体受热到100℃时失去结晶水,成为无水草酸。某学习小组的同学拟以甘蔗渣为原料用水解—氧化—水解循环进行制取草酸。
|
 请跟据以上信息回答下列问题:
请跟据以上信息回答下列问题:(1)图示①②的氧化—水解过程是在上图1的装置中进行的,指出装置A的名称 。
(2)图示①②的氧化—水解过程中,在硝酸用量、反应的时间等条件均相同的情况下,改变反应温度以考察反应温度对草酸收率的影响,结果如上图2所示,请选择最佳的反应温度为 ,为了达到图2所示的温度,选择图1的水浴加热,其优点是 。
(3)在图示③④中的操作涉及到抽滤,洗涤、干燥,下列有关说法正确的是 。
A.在实验过程中,通过快速冷却草酸溶液,可以得到较大的晶体颗粒,便于抽滤
B.在洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
C.为了检验洗涤是否完全,应拔下吸滤瓶与安全瓶之间橡皮管,从吸滤瓶上口倒出少量滤液于试管中进行相关实验。
D.为了得到干燥的晶体,可以选择在坩埚中直接加热,并在干燥器中冷却。
(4)要测定草酸晶体(H2C2O4·2H2O)的纯度,称取7.200g制备的草酸晶体溶于适量水配成250mL溶液,取25.00mL草酸溶液于锥形瓶中,用0.1000mol/L酸性高锰酸钾溶液滴定
(5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O),
①取25.00mL草酸溶液的仪器是 ,
②在草酸纯度测定的实验过程中,下列说法正确的是: 。
A.润洗滴定管时,应从滴定管上口加满所需的酸或碱液,使滴定管内壁充分润洗
B.移液管取草酸溶液时,需将尖嘴处的液体吹入锥形瓶,会使实验误差偏低
C.滴定时,左手轻轻向内扣住活塞,手心空握以免碰到活塞使其松动漏出溶液
D.滴定终点读取滴定管刻度时,仰视标准液液面,会使实验误差偏高
③判断滴定已经达到终点的方法是: 。
④达到滴定终点时,消耗高锰酸钾溶液共20.00mL,则草酸晶体的纯度为 。