题目内容
【题目】下列操作对应的现象和离子方程式均正确的是( )
操作 | 现象 | 离子方程式 | |
A | 饱和碳酸钠溶液中通入过量CO2 | 无明显变化 | CO |
B | 向苏打溶液溶液中滴加稀硫酸 | 立即产生气泡 | CO |
C | 向Ba(OH)2溶液中加足量NaHCO3溶液 | 生成白色沉淀 | 2HCO |
D | 向NaHCO3溶液中加入少量偏铝酸钠 | 生成白色沉淀和无色气体 | HCO |
A.AB.BC.CD.D
【答案】C
【解析】
A. 向饱和碳酸钠溶液中通入足量二氧化碳气体,有白色晶体析出,离子方程式:2Na++ CO![]() +CO2+H2O =2NaHCO3↓,故A错误;
+CO2+H2O =2NaHCO3↓,故A错误;
B. 向苏打溶液溶液中滴加稀硫酸,开始没有现象,后来产生气泡,离子方程式是: CO![]() +H+= HCO
+H+= HCO![]() ,HCO
,HCO![]() + H+= CO2↑+H2O,故B错误;
+ H+= CO2↑+H2O,故B错误;
C. 向Ba(OH)2溶液中加足量NaHCO3溶液,氢氧化钡少量,氢氧化钡电离出的钡离子和氢氧根离子完全反应,离子方程式是:2HCO![]() +Ba2++2OH-=BaCO3↓+2H2O+CO
+Ba2++2OH-=BaCO3↓+2H2O+CO![]() ,故C正确;
,故C正确;
D. 向NaHCO3溶液中加入少量偏铝酸钠,偏铝酸根离子促进碳酸氢根离子的电离,生成氢氧化铝白色沉淀和碳酸根离子,离子方程式是:HCO![]() +AlO
+AlO![]() +H2O=Al(OH)3↓+ CO
+H2O=Al(OH)3↓+ CO![]() ,故D错误;
,故D错误;
故选:C。

【题目】硫酸锌是制造锌钡白和锌盐的主要原料,也可用作木材的防腐剂等。用氧化锌烟尘(主要成分为ZnO,还含有少量PbO、CuO、Fe2 O3、FeO等)生产ZnSO4·7H2O的流程如下:
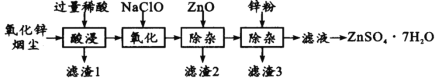
有关金属离子[c(Mn+)= 0.l mol/L]形成氢氧化物沉淀的pH范围如下表:
金属离 | Fe3+ | Fe2+ | Zn2+ | Cu2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 4.7 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 6.7 |
(1)“酸浸”时用的稀酸是____;滤渣1主要成分是____。
(2)“氧化”时的离子方程式为_________;加入ZnO除杂时溶液的pH控制范围是____~5.0。
(3)滤渣3含有锌和____;滤液得到ZnSO4·7H2O的操作是____、洗涤、干燥。
(4)取14.35gZnSO4·7H2O加热至不同温度,剩余固体的质量如下表
温度/℃ | 100 | 250 | 680 | 930 |
质量/g | 8. 95 | 8. 05 | 6. 72 | 4.05 |
则680℃时剩余固体的化学式为________(填序号)。
A.ZnO B.Zn3O(SO4