题目内容
7.下列说法错误的是( )| A. | 实验室制快速氨气可用浓氨水滴加到固体NaOH中 | |
| B. | 漂白粉的成分是NaCl与NaClO | |
| C. | 水玻璃应保存在具橡皮塞的玻璃试剂瓶中 | |
| D. | NO气体的收集不能用排空气法 |
分析 A.浓氨水易挥发,氢氧化钠溶解产生大量的热,且电离产生大量氢氧根离子;
B.漂白粉的成分是氯化钙和次氯酸钙;
C.玻璃中含有SiO2,易与氢氧化钠反应生成具有黏性的硅酸钠而使玻璃塞打不开;
D.一氧化氮与氧气反应.
解答 解:A.浓氨水易挥发,氢氧化钠溶解产生大量的热,且电离产生大量氢氧根离子,都能促进氨气的逸出,可以用来制备氨气,故A正确;
B.漂白粉的成分是氯化钙和次氯酸钙,故B错误;
C.玻璃中含有SiO2,易与氢氧化钠反应生成具有黏性的硅酸钠而使玻璃塞打不开,保存氢氧化钠溶液时不能用玻璃塞,应用橡皮塞,故C正确;
D.一氧化氮与氧气反应,空气的主要成分有氧气,所以不能用排气法收集,故D正确;
故选:B.
点评 本题考查了元素化合物知识,熟悉氨气、二氧化硅、一氧化氮的性质,熟悉漂白粉的成分是解题关键,题目难度不大.

练习册系列答案
相关题目
18.下列化学反应的离子方程式正确的是( )
| A. | 氯气与氢氧化钠溶液:Cl2+2OH-=Cl-+ClO-+H2O | |
| B. | 将少量金属钠放人冷水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O | |
| D. | 向澄清石灰水中通入过量二氧化碳:CO2+Ca2++2OH-=CaCO3↓+H2O |
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,18g(H218O)含有的原子总数为3NA | |
| B. | 标准状况下,4.2g CH2=CH2气体中所含有的碳原子总数为0.3NA | |
| C. | 将0.1mol的Cl2通入1L水中转移的电子数目为0.1NA | |
| D. | 0.1mol/LAl2(SO4)3溶液中含有的Al3+总数为0.2NA |
12.下列化工原料的选择符合绿色化学思想的是( )
| A. | 使用无毒无害的原料 | B. | 使用颜色为绿色的化工产品 | ||
| C. | 不使用任何化学物质 | D. | 使用不可再生的资源 |
 和
和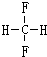
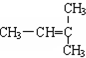 和CH2=CH-CH2
和CH2=CH-CH2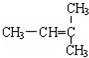 和
和
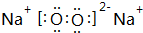 .
.
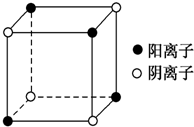 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1.请回答下列问题:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1.请回答下列问题: