题目内容
12.下列化工原料的选择符合绿色化学思想的是( )| A. | 使用无毒无害的原料 | B. | 使用颜色为绿色的化工产品 | ||
| C. | 不使用任何化学物质 | D. | 使用不可再生的资源 |
分析 “绿色化学”核心是利用化学原理从源头上减少和消除工业生产对环境的污染;反应物的原子全部转化为期望的最终产物,据此解答.
解答 解:A.使用无毒无害的原料可以从源头上消除污染,符合绿色化学的思想,故A正确;
B.使用颜色为绿色的化工产品,不能保证减少污染,不符合绿色化学思想,故B错误;
C.不使用任何化学物质不能进行化工生产,不符合客观实际,故C错误;
D.使用可再生的资源能够充分利用资源,符合绿色化学的思想,使用不可再生资源,不能充分利用资源,不符合绿色化学思想,故D错误;
故选:A.
点评 本题考查了绿色化学的含义,明确绿色化学的核心是解题关键,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
2.用CH4催化还原NO,可以消除氮氧化物的污,有望解决汽车尾气污染问题,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-akJ•mol-1
按上述转化,标准状况下44.8L NO2被还原至N2,整个过程中放出的热量为867kJ,则a的值为( )
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-akJ•mol-1
按上述转化,标准状况下44.8L NO2被还原至N2,整个过程中放出的热量为867kJ,则a的值为( )
| A. | 1160 | B. | 2308 | C. | 1441 | D. | 2320 |
3.禁止用工业酒精配制饮用酒,这是因为酒精中含有的少量有毒物质是( )
| A. | 甘油 | B. | 醋酸 | C. | 甲醇 | D. | 乙醛 |
7.下列说法错误的是( )
| A. | 实验室制快速氨气可用浓氨水滴加到固体NaOH中 | |
| B. | 漂白粉的成分是NaCl与NaClO | |
| C. | 水玻璃应保存在具橡皮塞的玻璃试剂瓶中 | |
| D. | NO气体的收集不能用排空气法 |
4.图表法、图象法是常用的科学研究方法.请回答以下问题
(1)第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
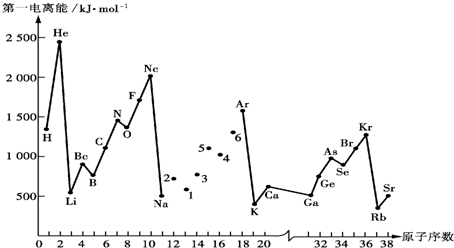
①将Na-Ar之间六种元素用短线连接起来(不必写在答题卷上),构成完整的图象.从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次减小
②上图折线中数字5代表元素在周期表中的位置是第三周期ⅤA族;
(2)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:试结合元素周期律知识完成下列问题:
①经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键(填离子键或共价键).
②某有机化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(3)已知:波长为300nm的紫外光的光子所具有的能量约为399kJ/mol.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
(1)第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.如图是部分元素原子的第一电离能I1随原子序数变化的曲线图.

①将Na-Ar之间六种元素用短线连接起来(不必写在答题卷上),构成完整的图象.从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次减小
②上图折线中数字5代表元素在周期表中的位置是第三周期ⅤA族;
(2)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:试结合元素周期律知识完成下列问题:
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
②某有机化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(3)已知:波长为300nm的紫外光的光子所具有的能量约为399kJ/mol.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
| C--C | C--N | C--S | |
| 键能 KJ/mol | 347 | 305 | 259 |
2.某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1mol/L)的用量均为2mL.
(1)该反应的化学方程式为5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
(3)某同学对实验①和②进行了三次实验测得以下实验数据(从混合振荡均匀开始计时):
计算用0.001mol•L-1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率:1×10-4mol?L-1?min-1.(忽略混合前后溶液的体积变化)
(4)某同学取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色.(反应热效应不明显,可忽略不计),该反应的反应速率迅速加快的主要原因可能是反应生成的MnSO4作为该反应的催化剂.
(1)该反应的化学方程式为5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 催化剂用量/g | KMnO4酸性溶液浓度mol/L | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对反应速率的影响 (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究催化剂对该反应速率的 影响; |
| ② | ||||
| ③ | 323 | |||
| ④ |
| KMnO4酸性溶液的浓度/mol•L-1 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
(4)某同学取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色.(反应热效应不明显,可忽略不计),该反应的反应速率迅速加快的主要原因可能是反应生成的MnSO4作为该反应的催化剂.

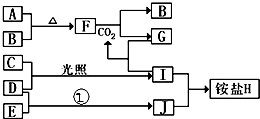 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种固氮反应.
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种固氮反应. .
. 2NH3的化学方程式.
2NH3的化学方程式.