题目内容
8.如图为离子晶体立体构型示意图:(●阳离子,○阴离子)以M代表阳离子,以N表示阴离子,写出各离子晶体的组成表达式不正确的是( )| A. | 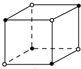 MN | B. | 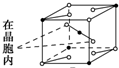 MN3 | C. |  MN2 | D. |  MN3 |
分析 A、图中阴阳离子个数=$\frac{1}{8}$×4=$\frac{1}{2}$,阴阳离子个数之比为1:1;
B、图中M离子个数=1+4×$\frac{1}{8}$=$\frac{3}{2}$,N离子个数=2+4×$\frac{1}{2}$+4×$\frac{1}{8}$=$\frac{9}{2}$;
C、图中M离子个数=$\frac{1}{8}$×4=$\frac{1}{2}$,N离子个数为1;
D、图中M离子个数4,N离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4;
阴阳离子个数之比等于其化学式中离子个数之比,据此判断化学式.
解答 解:A、图中阴阳离子个数=$\frac{1}{8}$×4=$\frac{1}{2}$,阴阳离子个数之比为1:1,其化学式为MN;
B、图中M离子个数=1+4×$\frac{1}{8}$=$\frac{3}{2}$,N离子个数=2+4×$\frac{1}{2}$+4×$\frac{1}{8}$=$\frac{9}{2}$,其化学式为MN3;
C、图中M离子个数=$\frac{1}{8}$×4=$\frac{1}{2}$,N离子个数为1,其化学式为MN2;
D、图中M离子个数4,N离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,其化学式为MN;
故选D.
点评 本题考查晶胞计算,侧重考查分析计算能力,正确判断离子被几个晶胞占有是解本题关键,题目难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
18.有关营养素的说法不正确的是( )
| A. | 营养素存在于不同的食物中 | |
| B. | 同种营养素在不同食物中的含量不同 | |
| C. | 不同个体每天需要的营养素的量是相同的 | |
| D. | 选择食物的原则是含营养素种类多、营养素含量丰富、容易被人体消化吸收和利用 |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 48克O2和O3的混合物含有氧原子数3NA | |
| B. | 22.4L甲烷(CH4)所含的原子数为5NA | |
| C. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA | |
| D. | 在20℃,1.01×105Pa(即在标准状况)时,11.2L氧气所含的原子数为NA |
16.化学与环境密切相关,下列有关说法正确的是( )
| A. | CO2属于大气污染物 | |
| B. | 酸雨是pH小于7的雨水 | |
| C. | 大气中CO2含量的增加会导致温室效应加剧 | |
| D. | CO2、NO2或SO2都会导致酸雨的形成 |
3.下列离子反应方程式表示正确的是( )
| A. | FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | |
| B. | 过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
13.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1 mol•L-1 HA溶液与0.1 mol•L-1 NaOH溶液混合至溶液呈中性:c(Na+)>c(A-) | |
| B. | 0.1 mol•L-1 HA溶液中:c(H+)=c(OH-)+c(A-) | |
| C. | 0.1 mol•L-1 NaA溶液中:c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液中加入少量NaA固体,HA的电离常数减小 |
20.下列各组表述中,两个微粒属于同种元素原子的是( )
| A. | M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2 的原子 | |
| B. | 2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5 | |
| C. | 3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2 | |
| D. | 最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p1的原子 |
17.据报道,某些花岗岩会产生放射性元素氡(${\;}_{86}^{222}$Rn),下列说法中不正确的是( )
| A. | 该原子的质量数为222 | B. | Rn是86号元素 | ||
| C. | 一个222 86Rn原子中有136个中子 | D. | 一个222 86Rn原子中有136个电子 |
18.正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.

发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据如下:
实验步骤如下:
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是滴液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%.

发生的反应如下:
CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据如下:
| 沸点/℃ | 密度(g.cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.5 | 0.8107 | 微溶 |
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.
②在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分.
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.
回答下列问题:
(1)B仪器的名称是滴液漏斗,D仪器的名称是直形冷凝管.
(2)沸石的作用是防止暴沸.
(3)将正丁醛粗产品置于分液漏斗中分液时,水在下层(填“上”或“下”)
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)本实验中,正丁醛的产率为51%.