题目内容
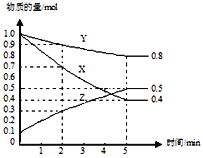
【题目】将10molA和5molB放入容积为10L的密闭容器中,某温度下发生反应:3A(g)+B(g)![]() 2C(g),在最初2s内,消耗A的平均速率为0.09mol·L-1·s-1,则在2s时,
2C(g),在最初2s内,消耗A的平均速率为0.09mol·L-1·s-1,则在2s时,
(1)容器中有___________molA;
(2)此时C的物质的量浓度为____________。
【答案】8.2 0.12mol/L
【解析】
3A(g)+B(g)![]() 2C(g)
2C(g)
起始量 1mol/L 0.5mol/L 0
变化量 0.18mol/L 0.06mol/L 0.12mol/L
平衡量 0.82mol/L 0.44mol/L 0.12mol/L
(1)容器中有:0.82mol/L×10L=8.2 molA。答案为:8.2
(2)此时C的物质的量浓度为0.12mol/L。答案为:0.12mol/L

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】一种以冷热镀管废料锌灰制ZnSO4·7H2O晶体,进而获取ZnO,并探索氢电极增压还原氧化锌电解法制锌的方法,工艺流程如图所示:
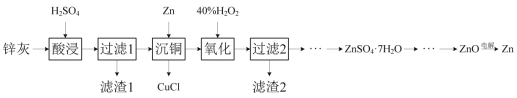
已知:①锌灰的主要成分为ZnO、ZnCl2,还含有SiO2、CuO、PbO和FeO。
②Cu++Cl-=CuCl↓
回答下列问题:
(1)滤渣1的主要成分为SiO2和___。
(2)酸浸时,硫酸浓度不能过高,原因是___。
(3)写出“沉铜”时的离子方程式___。
(4)在pH为5.6的条件下氧化后,再加入聚丙烯酰胺絮凝剂并加热搅拌,其目的是___。
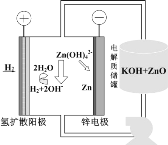
(5)氢电极增压还原氧化锌的装置如图所示,储罐内ZnO溶解后形成Zn(OH)![]() 离子,每溶解1molZnO需消耗___molKOH。电解池中的总反应离子方程式为:___。
离子,每溶解1molZnO需消耗___molKOH。电解池中的总反应离子方程式为:___。
(6)该工艺废水中含有Zn2+,排放前需处理。向废水中加入CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2++H2SZnS(s)+2H+。处理后的废水中部分微粒浓度为:
微粒 | H2S | CH3COOH | CH3COO- |
浓度/mol·L-1 | 0.10 | 0.05 | 0.10 |
处理后的废水的pH=___,c(Zn2+)=___。(已知:Ksp(ZnS)=1.0×10-23,Ka1(H2S)=1.0×10-7,Ka2(H2S)=1.0×10-14,Ka(CH3COOH)=2.0×10-5)