题目内容
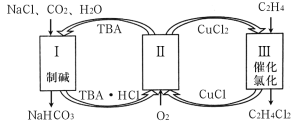
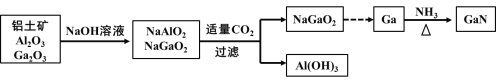
【题目】氮化镓(GaN)是制造LED的重要材料,被誉为“第三代半导体材料”。镓(31Ga)的氧化物和氢氧化物均为两性化合物,工业制备氮化镓的工艺流程如图所示。下列判断正确的是
A.Ga位于第五周期第IIIA族B.酸性:Al(OH)3>Ga(OH)3
C.Ga(OH)3可与NaOH反应生成NaGaO2D.Ga与NH3反应的另一种生成物可用作航天燃料
【答案】CD
【解析】
铝土矿中加入氢氧化钠,镓(31Ga)和铝的氧化物均为两性氧化物,故反应生成偏铝酸钠和NaGaO2,通入适量的二氧化碳后,偏铝酸钠优先与二氧化碳反应生成氢氧化铝,NaGaO2经过系列反应得到单质镓,最终与氨气反应生成GaN。
A. Ga的原子序数为31,位于第四周期第IIIA族,A错误;
B. 根据流程,将适量CO2通入NaAlO2和NaGaO2的混合液中得到Al(OH)3沉淀,说明CO2优先与NaAlO2反应,则酸性Al(OH)3<Ga(OH)3,B错误;
C.Ga的氧化物和氢氧化物均为两性化合物,且根据题中流程图可知,Ga(OH)3可与NaOH反应生成NaGaO2,C正确;
D. 根据元素守恒可知,Ga与NH3反应的另一种生成物为氢气,氢气具有可燃性,可用作航天燃料,D正确;
答案为CD。

 开心蛙口算题卡系列答案
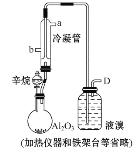
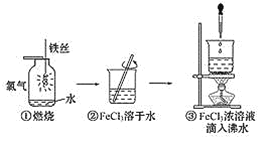
开心蛙口算题卡系列答案【题目】某化学实验小组将装有铜与浓硫酸烧瓶加热一段时间后,取出烧瓶中固体,探究其成分。查资料可知,浓硫酸与铜反应可能生成CuS或Cu2S,它们都难溶于水,能溶于稀硝酸。实验如下:
(i)用蒸馏水洗涤固体,得到蓝色溶液,固体呈黑色。
(ii)取少量黑色固体于试管中,加入适量稀硝酸,黑色固体逐渐溶解,溶液变为蓝色,产生无色气泡。取少量上层清液于试管,滴加氯化钡溶液,产生白色沉淀。
①根据实验(i)得到蓝色溶液可知,固体中含____________(填化学式)
②根据实验(ii)的现象_______(填“能”或“不能”)确定黑色固体是CuS还是Cu2S,理由是__________________________________________________________________________。
写出Cu2S与稀硝酸反应的化学方程式____________________________________________
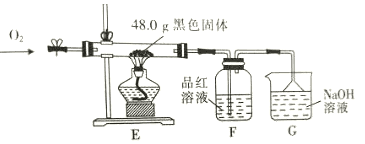
③为了进一步探究黑色固体的成分,将实验(i)中黑色固体洗涤、烘干,再称取48.0g黑色固体进行如下实验,通入足量O2,使硬质玻璃管中黑色固体充分反应,观察到F瓶中品红溶液褪色。
实验序号 | 反应前黑色固体质量/g | 充分反应后黑色固体质量/g |
I | 48.0 | 48.0 |
Ⅱ | 48.0 | 44.0 |
Ⅲ | 48.0 | 40.0 |
根据上表实验数据推测:实验I中黑色固体的化学式为_____________________________;实验Ⅱ中黑色固体的成分及质量为_______________________________________________。