题目内容
【题目】(1)碱洗铝材除其表面的氧化膜,碱洗时常有气泡冒出,原因是____(用离子方程式表示)。为将碱洗后溶液中的铝以沉淀形式回收,最好应加入下列试剂中的________(填字母)。
a.稀H2SO4b.盐酸 c.CO2d.氨水 e.NaOH
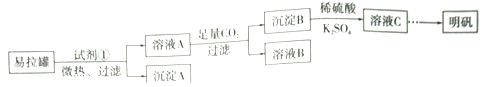
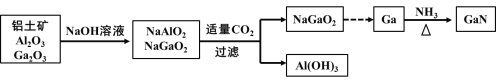
(2)已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:

①写出下列物质的化学式:X:___,A:____,B:___,C:_____。
②写出以下反应的离子方程式:A→B:_______;C→B:__________。
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑ c Al Al2O3 NaAlO2 AlCl3 Al2O3+2OH-=2AlO2-+H2O Al3++4OH-= AlO2-+2H2O
【解析】
(1)Al单质可以和碱反应生成氢气;偏铝酸盐中通入二氧化碳会生成沉淀,且沉淀不会溶解;
(2)X是某金属单质,X、A、B、C含同一种元素,由转化关系可知,X与NaOH反应,且A与NaOH反应,则X为Al,A为Al2O3,B为NaAlO2,C为AlCl3,然后结合物质的性质及化学用语来解答。
(1)Al单质可以和碱反应生成氢气,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;碱洗后Al元素主要以偏铝酸根的形式存在,加入盐酸和硫酸等强酸会先生成沉淀,当酸过量后沉淀会溶解,碱不和偏铝酸盐反应,故选用二氧化碳,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;c;
(2)①X是某金属单质,X、A、B、C含同一种元素,由转化关系可知,X与NaOH反应,且A与NaOH反应,则X为Al,A为Al2O3,B为NaAlO2,C为AlCl3,
故答案为:Al;Al2O3;NaAlO2;AlCl3;
②A为Al2O3,与强碱溶液反应生成偏铝酸盐和水,故答案为:Al2O3+2OH-=2AlO2-+H2O;
C为AlCl3,与过量氢氧化钠反应生成偏铝酸盐和水,故答案为:Al3++4OH-= AlO2-+2H2O。

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案