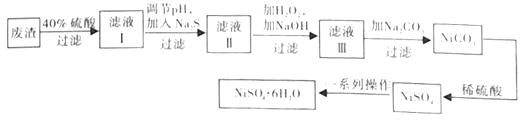
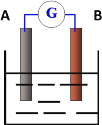
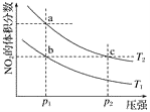
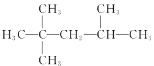��Ŀ����
����Ŀ��ij��ѧʵ��С�齫װ��ͭ��Ũ������ƿ����һ��ʱ���ȡ����ƿ�й��壬̽����ɷ֡������Ͽ�֪��Ũ������ͭ��Ӧ��������CuS��Cu2S�����Ƕ�������ˮ��������ϡ���ᡣʵ�����£�
��i��������ˮϴ�ӹ��壬�õ���ɫ��Һ������ʺ�ɫ��
��ii��ȡ������ɫ�������Թ��У���������ϡ���ᣬ��ɫ�������ܽ⣬��Һ��Ϊ��ɫ��������ɫ���ݡ�ȡ�����ϲ���Һ���Թܣ��μ��Ȼ�����Һ��������ɫ������
�ٸ���ʵ�飨i���õ���ɫ��Һ��֪�������к�____________���ѧʽ��
�ڸ���ʵ�飨ii��������_______����������������������ȷ����ɫ������CuS����Cu2S��������__________________________________________________________________________��
д��Cu2S��ϡ���ᷴӦ�Ļ�ѧ����ʽ____________________________________________
��Ϊ�˽�һ��̽����ɫ����ijɷ֣���ʵ�飨i���к�ɫ����ϴ�ӡ���ɣ��ٳ�ȡ48.0g��ɫ�����������ʵ�飬ͨ������O2��ʹӲ�ʲ������к�ɫ�����ַ�Ӧ���۲쵽Fƿ��Ʒ����Һ��ɫ��

ʵ����� | ��Ӧǰ��ɫ��������/g | ��ַ�Ӧ���ɫ��������/g |
I | 48.0 | 48.0 |
�� | 48.0 | 44.0 |
�� | 48.0 | 40.0 |
�����ϱ�ʵ�������Ʋ⣺ʵ��I�к�ɫ����Ļ�ѧʽΪ_____________________________��ʵ�����к�ɫ����ijɷּ�����Ϊ_______________________________________________��
���𰸡�CuSO4 ���� CuS��Cu2S�����ᷴӦ�IJ�����ͬ 3Cu2S+16HNO3+=3CuSO4+10NO��+3Cu(NO3)2+8H2O Cu2S Cu2S 24.0g��CuS 24.0g
��������
ϡ�������ǿ�����ԣ��ܰ�S��-2������Ϊ-6�ۣ���Cu��-1������Ϊ+2�ۣ������ᱻ��ԭΪNO��һ��ɫ���壬�ɴ˿���д��CuS��Cu2S��ϡ����ķ�Ӧ����ʽ��������У���Ϊ�漰�������ı仯��������Ҫ���Ƿ�Ӧǰ�������ʵ���Է��������ı仯���������������1��Cu2S����2��CuO��Cuԭ���غ㣩������Է�������û�з����仯����1��CuS����1��CuO��Cuԭ���غ㣩����Է���������С��16�����ò����������ƶϳ�������гɷּ���Ӧ��������
��������ˮϴ�ӹ��壬�õ���ɫ��Һ���������һ������CuSO4��
��CuS��Cu2S��ϡ���ᷴӦ�ķ���ʽ�ֱ�Ϊ��![]() ��
��![]() ��������Ӧ������ɫ��Һ����ɫ�������ɣ��Ҽ���BaCl2��Һ���а�ɫ�������ɣ��������жϺ�ɫ����ijɷ֣�
��������Ӧ������ɫ��Һ����ɫ�������ɣ��Ҽ���BaCl2��Һ���а�ɫ�������ɣ��������жϺ�ɫ����ijɷ֣�
��Fƿ��Ʒ����Һ��ɫ��˵����SO2���ɣ�����ͭԭ�Ӹ����غ㣬��
Cu2S-2CuO ��m=64��2+32-64��2-16��2=0��CuS-CuO ��m=64+32-64-16=16��
ʵ��I�У���Ӧǰ������������䣬��˵����ɫ������ֻ��Cu2S��
ʵ��II�У����������仯��Ϊ4.0g��������ƶϳ��������仯��CuS������
CuS-CuO ��m=16
96 �� �� 16
m(CuS) �� 4.0g
m(CuS)=![]() =24.0g
=24.0g
m(Cu2S)=48.0g-24.0g=24.0g
��ú�ɫ�����Ϊ24.0g��Cu2S��24.0g��CuS��